题目内容
12.写出微粒符号3$\stackrel{+3}{Fe}$Cl3中的“3”的意义,前面的“3”氯化铁分子的个数为3;上面的“3”氯化铁中铁元素的化合价为+3价;右下角的“3”1个氯化铁分子中含有3个氯原子.分析 标在分子符号前面的数字表示分子的个数,标在元素符号正上方的数字表示该元素化合价的数值,标在化学式中元素右下角的数字表示一个分子中所含原子的数目.
解答 解:标在分子符号前面的数字表示分子的个数,3$\stackrel{+3}{Fe}$Cl3中的“3”表示氯化铁分子的个数为3.
标在元素符号正上方的数字表示该元素化合价的数值,3$\stackrel{+3}{Fe}$Cl3中的“3”表示氯化铁中铁元素的化合价为+3价.标在化学式中元素右下角的数字表示一个分子中所含原子的数目,3$\stackrel{+3}{Fe}$Cl3中的“2”表示1个氯化铁分子中含有3个氯原子.
故答案为:氯化铁分子的个数为3;氯化铁中铁元素的化合价为+3价;1个氯化铁分子中含有3个氯原子.
点评 本题难度不大,主要考查了元素符号不同位置的数字表示的意义,掌握标在元素符号不同位置的数字所表示的意义是正确解答此类题的关键所在.

练习册系列答案
 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案
相关题目
3.某化学课外兴趣小组探究氢气还原氧化铜的反应,有如下实验装置:
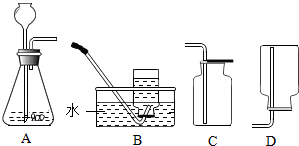
(1)上述A装置可用于实验室制取氢气和二氧化碳,请分别写出实验室制取氢气和二氧化碳的化学方程式Zn+H2SO4=ZnSO4+H2↑;CaCO3+2HCl=CaCl2+H2O+CO2↑;
上述可用于收集二氧化碳装置是C(用装置字母序号填空).
(2)请你参与探究氢气还原氧化铜得到的红色固体的成分,完成下列各题:
已知信息:Ⅰ.氢气还原氧化铜除生成铜外还可能生成氧化亚铜(Cu2O);Ⅱ.Cu和Cu2O均为不溶于水的红色固体;Ⅲ.Cu2O+H2SO4=CuSO4+Cu+H2O
提出问题:红色固体含有什么物质?
①猜想假设:
假设一:红色固体只含Cu;假设二:红色固体只含Cu2O;
假设三:红色固体含有Cu和Cu2O(请补充完成假设三).
②实验探究:(填写表中空格)
③数据处理:甲同学称取Wg红色固体加入到足量硫酸溶液中使其充分反应后,(填操作名称)、洗涤、干燥,称量剩余红色固体质量为mg,通过计算,若m=$\frac{64w}{144}$g(选填>、<或=),则假设二成立;若m<$\frac{64w}{144}$g(选填>、<或=),则假设三成立.
④交流与反思:只要假设合理,实验方法正确,根据实验现象和数据就能得出结论.

(1)上述A装置可用于实验室制取氢气和二氧化碳,请分别写出实验室制取氢气和二氧化碳的化学方程式Zn+H2SO4=ZnSO4+H2↑;CaCO3+2HCl=CaCl2+H2O+CO2↑;
上述可用于收集二氧化碳装置是C(用装置字母序号填空).
(2)请你参与探究氢气还原氧化铜得到的红色固体的成分,完成下列各题:
已知信息:Ⅰ.氢气还原氧化铜除生成铜外还可能生成氧化亚铜(Cu2O);Ⅱ.Cu和Cu2O均为不溶于水的红色固体;Ⅲ.Cu2O+H2SO4=CuSO4+Cu+H2O
提出问题:红色固体含有什么物质?
①猜想假设:
假设一:红色固体只含Cu;假设二:红色固体只含Cu2O;
假设三:红色固体含有Cu和Cu2O(请补充完成假设三).
②实验探究:(填写表中空格)
| 实验操作 | 实验现象 | 实验结论 |
| a.取少量红色固体加入到足量硫酸溶液中 | 无明显现象 | 假设成立假设一 |
| b.取少量红色固体加入到足量硫酸溶液中 | 有红色固体剩余 | 假设二和假设三均成立 |
④交流与反思:只要假设合理,实验方法正确,根据实验现象和数据就能得出结论.
20.呼吸作用及光合作用都离不开空气.下列关于空气的说法正确的是( )
| A. | 空气是一种化合物 | |
| B. | 空气是几种单质和几种化合物组成的混合物 | |
| C. | 新鲜的空气是纯净物 | |
| D. | 空气是几种元素的混合物 |
4.两包粉末,一是铁粉,二是氧化铜粉,快速将它们鉴别出来的方法是( )
| A. | 观察颜色,加以鉴别? | |
| B. | 分别加水溶解,加以鉴别? | |
| C. | 用磁铁吸引,加以鉴别 | |
| D. | 装入试管中分别加热,再分别通入H2观察现象,加以鉴别? |
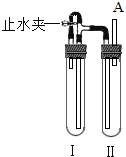 Fe(OH)3是一种红褐色沉淀,Fe(OH)2却是一种白色沉淀,它们都可以在水中通过发生复分解反应来制得,比如:FeCl3+NaOH═A↓+NaCl,则A沉淀是.由于Fe(OH)2不稳定,在水中,只要有一点氧气就极易发生反应生成Fe(OH)3,写出其反应的化学方程式:4Fe(OH)2+O2+2H2O=4Fe(OH)3,因而在溶液中较难制得纯净的Fe(OH)2.若按照常规的正确方法向FeCl2溶液中滴加NaOH溶液,很难观察到白色沉淀现象,只能看到灰绿色沉淀.
Fe(OH)3是一种红褐色沉淀,Fe(OH)2却是一种白色沉淀,它们都可以在水中通过发生复分解反应来制得,比如:FeCl3+NaOH═A↓+NaCl,则A沉淀是.由于Fe(OH)2不稳定,在水中,只要有一点氧气就极易发生反应生成Fe(OH)3,写出其反应的化学方程式:4Fe(OH)2+O2+2H2O=4Fe(OH)3,因而在溶液中较难制得纯净的Fe(OH)2.若按照常规的正确方法向FeCl2溶液中滴加NaOH溶液,很难观察到白色沉淀现象,只能看到灰绿色沉淀.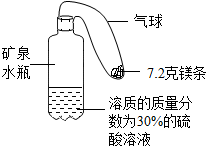 某实验小组同学设计了如图装置模拟氢气探空气球(装置中气球固定在矿泉水瓶上).将气球中的镁条加入到硫酸溶液中,恰好完全反应.
某实验小组同学设计了如图装置模拟氢气探空气球(装置中气球固定在矿泉水瓶上).将气球中的镁条加入到硫酸溶液中,恰好完全反应.