题目内容
14.如图中的①、②分别是氯元素、钠元素在周期表中的信息,A、B、C、D是四种粒子结构示意图.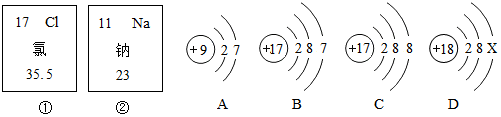
请你回答下列问题:
(1)钠元素的原子序数为11,氯元素的相对原子质量为35.45.
(2)示意图D中的x=8.
(3)A、B、C、D中属于同种元素的粒子是BC(填序号).
(4)已知A和B两种粒子的化学性质相似,是由于最外层电子数相同.
分析 (1)根据图中元素周期表可以获得的信息:左上角的数字表示原子序数;字母表示该元素的元素符号;中间的汉字表示元素名称;汉字下面的数字表示相对原子质量,进行分析解答.
(2)根据原子中,核内质子数与核外电子数之间的关系分析x的值;
(3)根据元素是质子数(即核电荷数)相同的一类原子的总称,决定元素种类的是质子数(即核电荷数)分析;
(4)元素的化学性质跟它的原子的最外层电子数目关系非常密切,最外层电子数相同的元素化学性质相似.
解答 解:(1)由元素周期表的信息可知,钠元素的原子序数为11,氯元素的相对原子质量为35.45;故填:11;35.45;
(2)在原子中,质子数=核外电子数,所以18+2+8+x,则x=8;故填:8;
(3)元素是质子数(即核电荷数)相同的一类原子的总称,同种元素的粒子是质子数相同,BC的核内质子数相同,属于同种元素.故填:BC;
(4)决定元素化学性质的是最外层电子数,原子的最外层电子数相同,具有相似的化学性质,由于A\B的最外层电子数均为7,故具有相似的化学性质.故填:最外层电子数相同.
点评 本题考查学生对在原子中,原子序数,质子数,核外电子数,核电荷数之间的关系及元素的最外层电子数决定元素的化学性质的理解与掌握.

练习册系列答案
相关题目
4.空气中含量最多、常充入食品袋作保护气的气体是( )
| A. | 氧气 | B. | 氮气 | C. | 二氧化碳 | D. | 稀有气体 |
5.氢气是1766年由卡文迪许在英国发现的,在点燃氢气前一定要检验其纯度.若晓敏想要在实验室中检验氢气的纯度,则她可选择的操作是( )
| A. | 闻气体的气味 | |
| B. | 用拇指堵住集满氢气的试管口,使试管口向下靠近火焰,移开拇指点火 | |
| C. | 用拇指堵住集满氢气的试管口,使试管口向上靠近火焰,移开姆指点火 | |
| D. | 将收集到的氢气通入水中检测其溶解度 |
19.下列实验操作错误的是( )
| A. |  滴加液体 | B. |  点燃酒精灯 | C. |  加热液体 | D. |  放置试管 |
 化学基础知识是学好化学的关键,请按下列要求填空.
化学基础知识是学好化学的关键,请按下列要求填空. 某元素是人体中的常量元素,它在人体内99%存在于骨骼和牙齿中.该元素的原子结构示意图如图:则该图中X的值为20,该原子化学性质较活泼(“活泼”或“稳定”),在化合物中的常见化合价为+2.
某元素是人体中的常量元素,它在人体内99%存在于骨骼和牙齿中.该元素的原子结构示意图如图:则该图中X的值为20,该原子化学性质较活泼(“活泼”或“稳定”),在化合物中的常见化合价为+2.