题目内容
14.某兴趣小组的同学用生铁制成的铁钉来制取晶体[FeSO4•7H2O],进行了如图实验: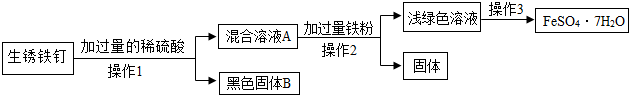
(1)操作1、2中所用的玻璃仪器有玻璃棒、烧杯、胶头滴管和漏斗.
(2)混合溶液A中的溶质有Fe2(SO4)3、H2SO4和FeSO4(化学式).
(3)操作3的步骤是加热浓缩、降温结晶、过滤、洗涤、干燥.
(4)洗涤[FeSO4•7H2O]晶体可下列试剂C.
A.水 B.稀硫酸 C.冷水.
分析 (1)操作1、2都是过滤,过滤能够把不溶于水的固体从液体中分离出来;
(2)稀硫酸和铁反应生成硫酸亚铁和氢气,和氧化铁反应生成硫酸铁和水;
(3)操作3的步骤是加热浓缩、降温结晶、过滤、洗涤、干燥;
(4)FeSO4•7H2O在冷水中的溶解度小于在通常情况下水中的溶解度.
解答 解:(1)操作1、2中都是过滤,过滤所用的玻璃仪器有玻璃棒、烧杯、胶头滴管和漏斗.
故填:漏斗.
(2)混合溶液A中的溶质有反应生成的硫酸亚铁、硫酸铁和过量的硫酸,硫酸铁、硫酸和硫酸亚铁的化学式分别是Fe2(SO4)3、H2SO4和FeSO4.
故填:FeSO4.
(3)操作3的步骤是加热浓缩、降温结晶、过滤、洗涤、干燥.
故填:降温结晶.
(4)利用稀硫酸洗涤FeSO4•7H2O时,会带入氢离子,FeSO4•7H2O在冷水中的溶解度小于在通常情况下水中的溶解度,因此洗涤时最好利用冷水.
故填:C.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案
相关题目
4.实验室有甲乙两种溶液,经测定,甲溶液的pH=0,乙溶液的pH=12.下列说法正确的是( )
| A. | 甲溶液呈中性,乙溶液呈碱性 | |
| B. | 甲溶液属于酸性溶液,乙溶液属于碱性溶液 | |
| C. | 甲溶液一定是酸性溶液,乙溶液一定是碱性溶液 | |
| D. | 甲溶液使无色酚酞变红色,乙溶液不能使无色酚酞变色 |
5.农作物生长需要含较多氮、磷、钾元素的化肥,下列化肥属于含磷复合肥料的是( )
| A. | NH4NO3 | B. | KNO3 | C. | (NH4)2HPO4 | D. | Ca(H2PO4)2 |
2.伊伐布雷定(C27H36N2O5)是世界上治疗心脏病的最新药物之一.下列有关伊伐布雷定的说法错误的是( )
| A. | 伊伐布雷定属于有机化合物 | B. | 伊伐布雷定分子由70个原子构成 | ||
| C. | 伊伐布雷定由4种元素组成 | D. | 伊伐布雷定的相对分子质量为468 |
9.下列图象分别与选项中的操作相对应,其中合理的是( )
| A. |  某温度下,向一定量不饱和硝酸钾溶液中不断加入硝酸钾晶体 | |
| B. |  向一定量的稀盐酸中逐滴滴加水 | |
| C. |  向一定量的氢氧化钠和碳酸钠的混合溶液中逐滴滴加盐酸 | |
| D. |  向一定量氯化铜溶液中加入一定量铝 |
6.河水出现水华的原因是( )
| A. | 水中氮磷元素大量增加 | B. | 水中缺少溶解氧 | ||
| C. | 水变黑发臭 | D. | 水中细菌大量增加 |
3.如图所示的实验,经过一段时间后,不能达到实验目的是( )
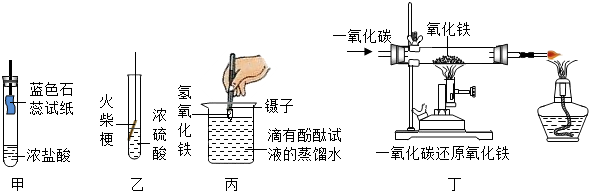

| A. | 甲图中,湿润的蓝色石蕊试纸变红色 | |
| B. | 乙图中,浸入浓硫酸中的火柴梗碳化变黑色 | |
| C. | 丙图中,将Fe(OH)3加入到滴有酚酞试液的蒸馏水中,溶液显红色 | |
| D. | 丁图中,红棕色的氧化铁粉末逐渐变成黑色 |
