题目内容
5.下列对分子、原子、离子的认识,正确的是( )| A. | 分子是化学变化中的最小粒子 | B. | 分子一定比原子大 | ||
| C. | 原子得失电子后形成离子 | D. | 溶质在水中均以离子形式存在 |
分析 A、根据在化学反应中,分子可以再分,原子在化学变化中不可再分解答;
B、根据分子和原子不能比较大小解答;
C、根据原子可以通过得失电子形成离子解答;
D、根据有些溶质以离子形式存在,有些以分子形式存在解答.
解答 解:
A、在化学反应中,分子可以再分,原子在化学变化中不可再分,错误;
B、分子和原子不能比较大小,错误;
C、原子通过得失电子能形成离子,正确;
D、有些溶质以离子形式存在;而蔗糖是由蔗糖分子构成的,溶质是以分子形式存在;故说法错误;
答案:C
点评 本题考查了物质的微观构成离子的知识,完成此题,可以依据微粒的性质进行.

练习册系列答案
相关题目
15.下列有关食品安全正确的是( )
| A. | 用工业石膏或医疗废弃石膏制作豆腐 | |
| B. | 炒菜中加入适量的加碘盐,预防地方性甲状腺肿大 | |
| C. | 在猪肉中加入大量的牛肉膏(一种添加剂),让猪肉有牛肉的口感 | |
| D. | 将地沟油和潲水油回收利用来炒菜,以达到变废为宝、节约资源的目的 |
12.下列现象中属于化学变化的是( )
| A. | 铁生锈 | B. | 石蜡熔化 | C. | 水变成水蒸气 | D. | 酒精挥发 |
19.某食品包装袋中有一个小纸袋,上面写“生石灰干燥剂,请勿食用”.该食品已放置两月有余.请你对下列问题进行探究.
(1)小纸袋中的物质能否继续作干燥剂?
(2)猜想:小纸袋中的物质除含有CaO外,还可能含有Ca(OH)2和CaCO3;
(3)请设计实验证明(2)中你所填的物质是否存在.加入足量的盐酸,观察是否产生气泡.
(1)小纸袋中的物质能否继续作干燥剂?
| 实验步骤 | 实验现象 | 结论 |
| 取足量的小纸袋中的固体放入烧杯中,加入适量的水,触摸杯壁 | 杯壁变热 | 可继续作干燥剂 |
(3)请设计实验证明(2)中你所填的物质是否存在.加入足量的盐酸,观察是否产生气泡.
10.用数轴表示某些化学知识直观、简明、易记.下列数轴表示的化学知识不正确的是( )
| A. | 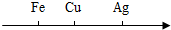 金属活动性由强到弱 | |
| B. |  液体的pH值由低到高 | |
| C. | 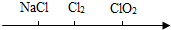 氯元素的化合价由低到高 | |
| D. | 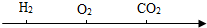 常温常压下气体在水中的溶解性由弱到强 |
14.下列物质属于混合物的是( )
| A. | 氧化钙 | B. | 医用酒精 | C. | 四氧化三铁 | D. | 高锰酸钾 |
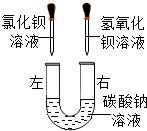 某化学活动小组在一次实验中进行了如图所示实验:此时观察到的实验现象是U形玻璃管左、右两端均产生白色沉淀;实验后,小组同学充分振荡U形玻璃管,将U形玻璃管内的物质过滤后,对滤液成分产生了浓厚的兴趣,进行了进一步的探究活动
某化学活动小组在一次实验中进行了如图所示实验:此时观察到的实验现象是U形玻璃管左、右两端均产生白色沉淀;实验后,小组同学充分振荡U形玻璃管,将U形玻璃管内的物质过滤后,对滤液成分产生了浓厚的兴趣,进行了进一步的探究活动