题目内容
9.为了配制50g溶质质量分数为4%的氯化钠溶液,需进行如下操作:①计箅;②用托盘天平称量2g氯化钠;③用50(选填“10mL”或“50mL”)量筒量取48mL水;④将两者置于烧杯中,用玻璃棒搅拌.分析 利用溶质质量=溶液质量×溶质的质量分数,溶剂质量=溶液质量-溶质质量,结合量筒的使用方法进行分析解答.
解答 解:溶质质量=溶液质量×溶质的质量分数,配制50g溶质质量分数为4%的氯化钠溶液,需氯化钠的质量=50g×4%=2g;溶剂质量=溶液质量-溶质质量,则所需水的质量=50g-2g=48g(合48mL).应用规格为50mL的量筒量取水的体积.
故答案为:2;50;48.
点评 本题难度不大,掌握溶质质量=溶液质量×溶质的质量分数、溶剂质量=溶液质量-溶质质量是正确解答本题的关键.

练习册系列答案
相关题目
11.“归纳与比较”是化学学习的主要方法.下列关于CO2与CO的不同点比较错误的是( )
| A. | 构成:一个二氧化碳分子比一个一氧化碳分子多一个氧原子 | |
| B. | 性质:CO2能溶于水,与水反应生成碳酸;CO难溶于水,但能燃烧 | |
| C. | 用途:CO2可用于光合作用、灭火等,会污染空气; CO可作燃料,不会污染空气 | |
| D. | 危害:CO2会造成“温室效应”; CO易与血液中的血红蛋白结合引起中毒 |
17.下列实验设计正确的是( )
| A. | 用带火星木条区分O2和CO2 | |
| B. | 用过滤的方法分离蔗糖和食盐 | |
| C. | 用托盘天平称取5.62g高锰酸钾 | |
| D. | 空气中氧气体积分数测定实验选用木炭作可燃物 |
1.小燕同学复习时整理了一些化学知识:
①过滤后液体仍然浑浊,原因可能是滤纸破损;
②氧气在氧化反应中提供氧,它具有氧化性;
③最外层电子为8的粒子一定是稀有气体原子;
④由一种元素组成的物质一定是单质;
⑤固体药品一般保存在细口瓶中;
⑥在书写具有保存价值的档案时,规定应使用碳素墨水,是因为在常温下碳的化学性质不活泼.
其中正确的是( )
①过滤后液体仍然浑浊,原因可能是滤纸破损;
②氧气在氧化反应中提供氧,它具有氧化性;
③最外层电子为8的粒子一定是稀有气体原子;
④由一种元素组成的物质一定是单质;
⑤固体药品一般保存在细口瓶中;
⑥在书写具有保存价值的档案时,规定应使用碳素墨水,是因为在常温下碳的化学性质不活泼.
其中正确的是( )
| A. | ①②⑥ | B. | ①③⑥ | C. | ③④⑤ | D. | ①④⑥ |
18.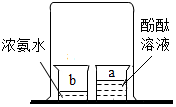 如图所示,在a烧杯中盛有酚酞溶液,在b烧杯中盛有浓氨水,有关现象和解释或结论正确的是( )
如图所示,在a烧杯中盛有酚酞溶液,在b烧杯中盛有浓氨水,有关现象和解释或结论正确的是( )
 如图所示,在a烧杯中盛有酚酞溶液,在b烧杯中盛有浓氨水,有关现象和解释或结论正确的是( )
如图所示,在a烧杯中盛有酚酞溶液,在b烧杯中盛有浓氨水,有关现象和解释或结论正确的是( ) | 选项 | 现象 | 解释或结论 |
| A | a烧杯溶液变红色 | 证明酚酞有挥发性 |
| B | a烧杯溶液变红色 | b中氨分子运动到a中,溶于水使酚酞变红 |
| C | b烧杯溶液为无色 | a中酚酞分子没有运动 |
| D | b烧杯溶液为无色 | 证明a、b中分子存在间距 |
| A. | A | B. | B | C. | C | D. | D |
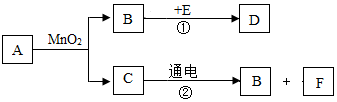 A-F是初中常见的6种物质,它们有如图所示的转化关系.已知A、C是无色液体,B、D、F是无色气体,其中大量排放D会引起温室效应,E是黑色固体.
A-F是初中常见的6种物质,它们有如图所示的转化关系.已知A、C是无色液体,B、D、F是无色气体,其中大量排放D会引起温室效应,E是黑色固体.