题目内容
用63.2克高锰酸钾加热制取方法可制得氧气多少克?(写出计算过程)
【答案】分析:利用高锰酸钾受热分解的化学方程式,根据高锰酸钾的质量求出氧气的质量.
解答:解:设可制得氧气的质量为x
2KMnO4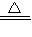 K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑
316 32
63.2g x
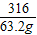 =
=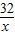
解得:x=6.4g
答:用63.2克高锰酸钾加热制取方法可制得氧气6.4克.
点评:利用化学方程式计算,首先必须读懂题意,然后根据化学方程式的计算步骤进行.注意的要点有:正确地写出反应的化学方程式、准确的计算出相关物质的相对分子质量、化学方程式中任意两种物质之间都存在固定的比例关系,解题的过程要规范.
解答:解:设可制得氧气的质量为x
2KMnO4
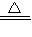 K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑316 32
63.2g x
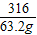 =
=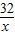
解得:x=6.4g
答:用63.2克高锰酸钾加热制取方法可制得氧气6.4克.
点评:利用化学方程式计算,首先必须读懂题意,然后根据化学方程式的计算步骤进行.注意的要点有:正确地写出反应的化学方程式、准确的计算出相关物质的相对分子质量、化学方程式中任意两种物质之间都存在固定的比例关系,解题的过程要规范.

练习册系列答案
相关题目