题目内容
10.小华同学用排水法收集了一大瓶沼气池中气体(图1中的A),为了弄清它的成分,进行了有关实验.请你与他一起完成以下探究活动:【对气体猜想】
猜想I:全部是CH4;
猜想Ⅱ:全部是CO;
猜想Ⅲ:是CO和CO2的混合气体;
猜想Ⅳ:是CH4和CO2的混合气体.
【实验和推断】将A中的气体依次通入B、C中,在D处点燃.
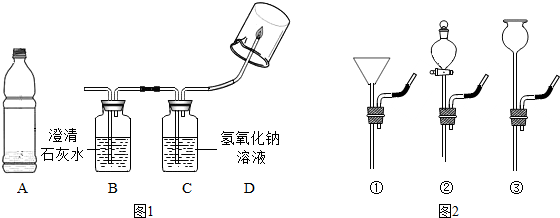
(1)要将A中的气体通入后面的装置中,应选图2中的② (填序号)“注水装置”.
(2)若B中石灰水变浑浊,则说明A中的气体中含有二氧化碳气体.
(3)装置C作用是除去气体中的CO2.
(4)若D处倒扣的是涂有澄清石灰水的烧杯,出现浑浊,且B中无明显现象,则“猜想I、Ⅱ”可能成立;若D处倒扣的是干冷的大烧杯,杯壁有水雾出现,有同学认为“猜想I、Ⅳ”可能成立,另有同学认为此现象不能证明收集到的气体中一定含有CH4,理由是气体通过B、C装置时,会带入水蒸气;要排除这种干扰可采取的措施是在点燃前将气体先通过干燥装置.
(5)采取(4)中的排除干扰措施后:若D处分别倒扣干冷的烧杯和涂石灰水的烧杯,分别出现水雾和浑浊,且B中也出现浑浊,则证明“猜想IV”成立.
分析 (1)根据①②③装置的差异性以及该实验的要求进行分析解答;
(2)根据澄清石灰水常用来检验二氧化碳的存在;
(3)根据氢氧化钠会与二氧化碳反应,可以用来吸收二氧化碳;
(4)根据BD中出现的现象进行分析,检验水的存在,需要先干燥气体;
(5)根据BD中的现象验证验证猜想的正确性.
解答 解:(1)要将A中的气体通入后面的装置中,应选图2中的带有分液漏斗的“注水装置”;
(2)若B中石灰水变浑浊,则说明A中的气体中含有CO2气体;
(3)装置C作用是除去气体中的CO2,以免干扰后面的实验;
(4)若D处倒扣的是涂有澄清石灰水的烧杯,出现浑浊,且B中无明显现象,则气体可能全部是CH4,也可能全部是CO,因为甲烷和一氧化碳燃烧都能够生成二氧化碳,因此“猜想”I、Ⅱ可能成立;
另有同学认为此现象不能证明收集到的气体中一定含有CH4,理由是气体通过B、C装置时,会带入水蒸气;
要排除这种干扰可采取的措施是在点燃前将气体先通过干燥装置;
(5)采取(4)中的排除干扰措施后,若D处分别倒扣干冷的烧杯和涂石灰水的烧杯,出现水雾和浑浊,说明气体中含有甲烷,B中也出现浑浊,说明气体中含有二氧化碳,从而证明“猜想IV”成立.
故答案为:(1)②;
(2)CO2;
(3)除去气体中的CO2;
(4)I、Ⅱ;气体通过B、C装置时,会带入水蒸气;在点燃前将气体先通过干燥装置;
(5)IV.
点评 利用所要鉴别物质的性质差别,设计实验,实验中出现明显的现象差异,达到鉴别物质的目的,还要注意干扰因素的存在.

练习册系列答案
 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案
相关题目
2. 小明买了一种“汽泡爽”的冲调饮料.
小明买了一种“汽泡爽”的冲调饮料.
(1)小明阅读资料发现:“汽泡爽”原料中的柠檬酸和小苏打(NaHCO3)粉末混合后加水,可以发生以下反应,请填写柠檬酸的化学式.
3NaHCO3+C6H8O7═C6H5O7Na3+3H2O+3CO2↑
(2)小明想探究加入的水的温度对产生气体量的影响,小明设计了如表实验方案.
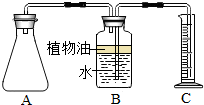
在老师的帮助下,小明采用相同的两套实验装置(如图)分别完成上述实验,在A中加入水,再加入一袋“汽泡爽”,迅速塞紧胶塞.量筒C用于收集A中产生的气体所排出的液体,冷却至室温后读取数据.B中油层的作用是防止二氧化碳溶解在B装置的水中.
(3)通过实验,小明测得:a=64mL,b=132mL,由此获得结论:“汽泡爽”产生气体的量与加水温度有关系.但是老师看到小明的实验报告后却指出:两套装置中,“汽泡爽”产生气体的总量应该近似相等,与温度关系不大,其本质原因是温度高气体在水中的溶解度小,收集到的气体多.
(4)通过反思,为了证明老师的观点,小明继续利用(3)中已反应完的两套装置,又做了一步实验,发现两套装置最终收集到的气体的总量确实相近,他的实验操作是将装置1反应后的液体温度升高到50℃,继续收集气体并测量体积.
 小明买了一种“汽泡爽”的冲调饮料.
小明买了一种“汽泡爽”的冲调饮料.(1)小明阅读资料发现:“汽泡爽”原料中的柠檬酸和小苏打(NaHCO3)粉末混合后加水,可以发生以下反应,请填写柠檬酸的化学式.
3NaHCO3+C6H8O7═C6H5O7Na3+3H2O+3CO2↑
(2)小明想探究加入的水的温度对产生气体量的影响,小明设计了如表实验方案.
| 实验序号 | 加入水的体积 | 加入水的温度 | 收集到的气体的体积 |
| 1 | 200mL | 15℃ | a(待记录) |
| 2 | 200mL | 50℃ | b(待记录) |
(3)通过实验,小明测得:a=64mL,b=132mL,由此获得结论:“汽泡爽”产生气体的量与加水温度有关系.但是老师看到小明的实验报告后却指出:两套装置中,“汽泡爽”产生气体的总量应该近似相等,与温度关系不大,其本质原因是温度高气体在水中的溶解度小,收集到的气体多.
(4)通过反思,为了证明老师的观点,小明继续利用(3)中已反应完的两套装置,又做了一步实验,发现两套装置最终收集到的气体的总量确实相近,他的实验操作是将装置1反应后的液体温度升高到50℃,继续收集气体并测量体积.
15.实验室可利用碱式碳酸铜[化学式:Cu2(OH)2CO3]制备氧化铜,并进行碳粉还原氧化铜的实验.(已知C中装有白色粉末状无水硫酸铜,遇水能变成蓝色固体CuSO4•5H2O)
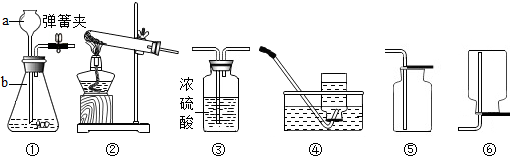
①制备氧化铜并检验产物,装置如图1所示(省略夹持仪器):

步骤一:连接A和B,打开活塞,通入空气.
步骤二:关闭活塞,连上C和D,开始加热.
步骤三:在加热过程中,记录在B中固体质量变化如下表,在t3时停止加热.
B中发生反应的化学方程式为::□Cu2(OH)2CO3$\frac{\underline{\;\;△\;\;}}{\;}$□CuO+□H2O+□CO2↑
(1)请在□中填入配平后的系数.1211
(2)A的作用是吸收空气中的吸收空气中的二氧化碳和水蒸气
(3)选择t3时停止加热的理由是固体质量不再减少,证明碱式碳酸铜已经完全分解
(4)根据上表数据可计算出玻璃管中原Cu2(OH)2CO3的质量为6.63g.
②一定量碳粉还原①中制得的氧化铜并检验产物是否有CO2生成,装置如图2所示:
(5)实验过程中,观察到F中溶液变浑浊,反应完全后,若仅撤走酒精喷灯停止加热,可能导致的后果是F中的液体通过导管流入E中,造成试管炸裂
(6)分析:若①中省略步骤三,对②中反应产物判断可能产生的影响及其原因.③不能确定炭粉还原氧化铜的生成物中是否含有二氧化碳.因为可能有①中未分解的碱式碳酸铜在实验②中分解,产生二氧化碳气体,干扰对炭粉还原氧化铜反应生成物的判断..
①制备氧化铜并检验产物,装置如图1所示(省略夹持仪器):

步骤一:连接A和B,打开活塞,通入空气.
步骤二:关闭活塞,连上C和D,开始加热.
步骤三:在加热过程中,记录在B中固体质量变化如下表,在t3时停止加热.
| 加热时间(min) | 0 | t1 | t2 | t3 |
| 玻璃管及其中固体质量(g) | 56.66 | 55.20 | 54.80 | 54.80 |
(1)请在□中填入配平后的系数.1211
(2)A的作用是吸收空气中的吸收空气中的二氧化碳和水蒸气
(3)选择t3时停止加热的理由是固体质量不再减少,证明碱式碳酸铜已经完全分解
(4)根据上表数据可计算出玻璃管中原Cu2(OH)2CO3的质量为6.63g.
②一定量碳粉还原①中制得的氧化铜并检验产物是否有CO2生成,装置如图2所示:
(5)实验过程中,观察到F中溶液变浑浊,反应完全后,若仅撤走酒精喷灯停止加热,可能导致的后果是F中的液体通过导管流入E中,造成试管炸裂
(6)分析:若①中省略步骤三,对②中反应产物判断可能产生的影响及其原因.③不能确定炭粉还原氧化铜的生成物中是否含有二氧化碳.因为可能有①中未分解的碱式碳酸铜在实验②中分解,产生二氧化碳气体,干扰对炭粉还原氧化铜反应生成物的判断..
2.实验室里,可以直接在酒精灯上加热的仪器为( )
| A. | 圆底烧瓶 | B. | 烧杯 | C. | 燃烧匙 | D. | 锥形瓶 |
19.自然界中最坚硬的物质是( )
| A. | 金刚石 | B. | 铁丝 | C. | 铝丝 | D. | 铜丝 |
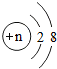 中,若n为不同数值可表示核外电子排布相同的不同微粒.
中,若n为不同数值可表示核外电子排布相同的不同微粒.