题目内容
11.水是常见的物质,请根据水的知识填空.(1)自然界中的水都不是纯水,欲除去水中不溶性杂质,需进行过滤操作,该操作过程中玻璃棒所起的作用是引流;自来水厂在净水时加入明矾,目的是吸附水中悬浮杂质使其吸附沉降.
(2)净水器中活性炭起吸附作用.
(3)日常生活中可以用肥皂水区分硬水和软水;生活中是如何把硬水转化成软水煮沸.
分析 (1)根据玻璃棒的作用分析;根据明矾的特性进行分析;
(2)根据活性炭具有吸附性解答;
(3)根据硬水和软水的鉴别方法分析加入的物质,生活中常用煮沸的方法来降低水的硬度,消毒杀菌解答;
解答 解:(1)在过滤时,玻璃棒的作用是引流;明矾溶于水生成的胶状物具有吸附小颗粒泥尘的作用,是常用的絮凝剂;
(2)净水器中活性炭起吸附作用;
(3)区分软水和硬水常用的物质是肥皂水.向待检验水中加入少量的肥皂水,搅拌,泡沫丰富的为软水,泡沫很少的为硬水.
生活中常用煮沸的方法,既可降低水的硬度,又能消毒杀菌;
故答案为:
(1)引流;吸附水中悬浮杂质使其吸附沉降;
(2)吸附;
(3)肥皂水、煮沸
点评 本题考查了净化水的知识和常用仪器的用途等知识,完成此题,可以依据已有的课本知识进行,要求同学们加强对基础知识的储备,以便灵活应用.

练习册系列答案
 课课练江苏系列答案
课课练江苏系列答案 名牌中学课时作业系列答案
名牌中学课时作业系列答案
相关题目
1.往AgNO3、Hg(NO3)2、Zn(NO3)2的混合溶液中加入一些铁粉,待反应完成后再过滤,不可能存在的情况是( )
| A. | 滤纸上有Ag,滤液中有Hg2+、Zn2+、Fe2+ | |
| B. | 滤纸上有Ag、Hg,滤液中有Zn2+、Fe2+ | |
| C. | 滤纸上有Ag、Hg、Fe,滤液中有Zn2+、Fe2+ | |
| D. | 滤纸上有Ag、Hg、Fe、Zn,滤液中有Zn2+、Fe2+ |
2.下列图象分别与选项中的操作相对应,其中不合理的是( )
| A. | 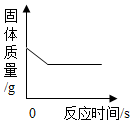 加热一定质量的小苏打固体,试管内固体的质量变化 | |
| B. | 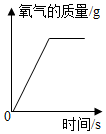 用向上排空气法收集一瓶氧气,集气瓶内氧气质量 | |
| C. |  等质量的锌粉和锌粒分别与相同浓度且足量的稀硫酸反应 | |
| D. | 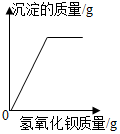 向硫酸和硫酸钠混合溶液中不断滴加氢氧化钡溶液 |
19.“防火胜于救火”,科学认识燃烧,增强安全防范意识是每个公民应具备的安全素养之一.下列说法错误的是( )
| A. | 身上着火不可乱跑,要就地打滚使火熄灭 | |
| B. | 水能灭火,是因为水能降低可燃物的着火点 | |
| C. | 夜间发现煤气泄漏,千万不能使用排油烟机等用电设施 | |
| D. | 油库、面粉厂和煤矿的坑道内要严禁烟火,以避免爆炸的发生 |
6.下列物质中,铁元素的化合价最低的是( )
| A. | Fe | B. | Fe2O3 | C. | FeSO4 | D. | FeO |
16.应用守恒思想解决下列相关问题,得到的推论正确的是( )
| A. | 葡萄糖燃烧生成二氧化碳和水,根据元素守恒推出:葡萄糖由碳、氢、氧三种元素组成 | |
| B. | 水电解生成H2和O2的分子数比为2:1,根据原子守恒推出:水分子中H、O原子个数比为2:1 | |
| C. | 100ml30%的浓盐酸用100 ml水稀释,根据溶质守恒推出:稀盐酸中溶质质量分数为15% | |
| D. | 18克碳与32 克氧气反应,根据质量守恒推出:生成二氧化碳的质量为50克 |
20.下列图象与对应选项关系合理的是.
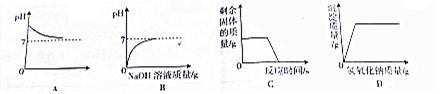

| A. | 常温下向pH=10的KOH溶液中不断加入水稀释 | |
| B. | 向一定溶质质量分数的盐酸中滴加氢氧化钠溶液至过量 | |
| C. | 表示煅烧一定质量的石灰石 | |
| D. | 向一定量硫酸和硫酸铜混合溶液中滴入氢氧化钠溶液 |
1.已知碳酸钙在高温下可分解生成氧化钙和二氧化碳,反应的化学方程式为:CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑,同学们从山上采集到一种石灰石(主要成分为碳酸钙),他们取80g该样品进行煅烧实验(所含杂质在煅烧过程中不发生变化),测得反应后固体的质量与反应时间的关系如下表:
请回答下列问题:
(1)当石灰石完全反应后,生成CO2的质量为22克.
(2)求该石灰石中含CaCO3的质量分数(写出计算过程).
| 反应时间∕s | t0 | t1 | t2 | t3 | t4 | t5 | t6 |
| 反应后固体的质量∕g | 80 | 75 | 70 | 66 | 62 | 58 | 58 |
(1)当石灰石完全反应后,生成CO2的质量为22克.
(2)求该石灰石中含CaCO3的质量分数(写出计算过程).
 看图回答下列问题.
看图回答下列问题.