题目内容
13.黄铜样品中铜的质量,取10g黄铜样品加入到100g稀硫酸中,恰好完全反应,产生氢气0.1g,求该黄铜中铜的质量?分析 根据金属活动性顺序,铜与硫酸不反应,利用锌与硫酸反应的化学方程式,根据氢气的质量求出锌的质量,进而求出铜的质量.
解答 解:根据金属活动性顺序,铜与硫酸不反应
设产生0.1g氢气消耗Zn的质量为x.
Zn+H2SO4=ZnSO4+H2↑
65 2
x 0.1g
$\frac{65}{x}=\frac{2}{0.1g}$
解得x=3.25g
所以铜的质量=10g-3.25g=6.75g
答案:该黄铜中铜的质量为6.75g
点评 掌握根据化学方程式的计算方法是正确解答本题的关键.

练习册系列答案
相关题目
4.世界每年因锈蚀而损失的金属数量巨大,防止金属锈蚀以成为科学研究中的重大问题.下列有关金属锈蚀与保护措施中不正确的是( )
| A. | 铁锈蚀发生了缓慢氧化 | |
| B. | 同样的铁制品在海南比在兰州更易锈蚀 | |
| C. | 铝的抗锈蚀性能比铁强,铝的金属活动性也比铁强 | |
| D. | 铝的抗锈蚀性能比铁强,生活中可用钢丝球洗刷铝锅 |
18.常温下将铁片分别放入下列物质中,观察不到明显现象的是( )
| A. | 蒸馏水 | B. | 稀硫酸 | C. | 稀盐酸 | D. | 硫酸铜溶液 |
5.下列有关实验结果的推测正确的是( )
| A. | 用过氧化氢制氧气时,若二氧化锰用量偏少则所得氧气质量会偏少 | |
| B. | 测定空气中氧气含量时,若红磷量不足则测得氧气的含量会偏大 | |
| C. | 配制10%的食盐水时,若仰视读取水的体积则所配溶液的浓度会偏大 | |
| D. | 制取二氧化碳时,若用浓盐酸则制得的气体通入石灰水有可能不变浑浊 |
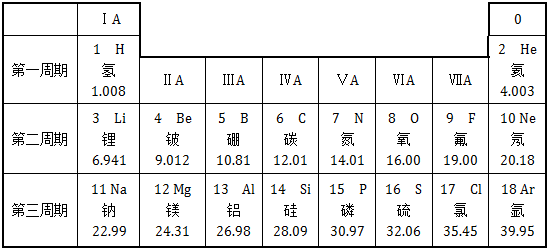
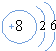 ,该微粒是元素周期表中的氧元素,它的核电荷数是8,碳元素的核电荷数是6,由此可知不同元素的本质区别是核电荷数不同.
,该微粒是元素周期表中的氧元素,它的核电荷数是8,碳元素的核电荷数是6,由此可知不同元素的本质区别是核电荷数不同.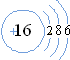 ,在化学反应中易得(填“得”或“失”)电子,是非金属(填“金属”或“非金属”)元素.则硫形成的离子符号为S2-
,在化学反应中易得(填“得”或“失”)电子,是非金属(填“金属”或“非金属”)元素.则硫形成的离子符号为S2-