题目内容
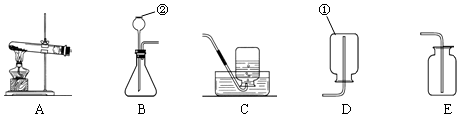
19.有一混合气体,其中可能含有O2、SO2和CO2中的一种或几种,某兴趣小组同学为确定其成分,查阅资料得知二氧化硫能使紫色的高锰酸钾溶液褪色,还能使澄清的石灰水变浑浊.他们设计的实验装置如图: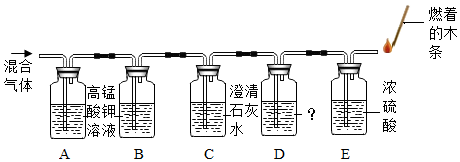
实验时观察到:A装置中紫色溶液褪色;C装置中澄清石灰水变浑浊.试回答下列问题:
(1)若混合气体含有较多氧气,实验中在装置E的出管口用燃着的木条检验,观察到的现象是燃着的木条燃烧的更旺.
(2)装置D中应装氢氧化钙(或氢氧化钠)溶液,装置E中浓硫酸的作用是除去混合气体中的水蒸气.
(3)SO2和CO2都能使澄清的石灰水变浑浊,到底混合气体中有没有CO2呢?如果你是老师,你可指导他们:除了D中澄清石灰水变浑浊外,还应观察到B中高锰酸钾溶液不褪色现象,才能确定混合气体中有CO2.
分析 (1)氧气具有助燃性,能使燃着的木条燃烧的更旺;(2)D中放氢氧化钙溶液,看二氧化碳是否被除净;浓硫酸具有吸水性,浓硫酸的作用是除去混合气体中的水蒸气;(3)根据二氧化硫能使紫色的高锰酸钾溶液褪色进行分析.
解答 解:(1)氧气具有助燃性,能使燃着的木条燃烧的更旺,混合气体通过ABCDE后已经将二氧化硫、二氧化碳、水蒸气都除掉,所以从E口出来的是纯净的氧气,能使燃着的木条燃烧的更旺;
(2)D中放氢氧化钙溶液(或氢氧化钠溶液),看二氧化碳是否被除净(为了除去二氧化碳);浓硫酸具有吸水性,浓硫酸的作用是除去混合气体中的水蒸气;
(3)根据二氧化硫能使紫色的高锰酸钾溶液褪色,A中高锰酸钾溶液褪色,是为了验证混合气体中含有二氧化硫,且除掉二氧化硫,B中高锰酸钾溶液不褪色,说明二氧化硫已经被除净,再通过澄清石灰水变浑浊,说明混合气体中含有二氧化碳.
故答案为:(1)燃着的木条燃烧的更旺;(2)氢氧化钙(或氢氧化钠);除去混合气体中的水蒸气;(3)B中高锰酸钾溶液不褪色.
点评 本题主要考查二氧化硫和二氧化碳的性质区别与联系,还有质量守恒定律的应用,锻炼了学生的综合分析解决问题的能力,和应变拓展能力.

练习册系列答案
 星级口算天天练系列答案
星级口算天天练系列答案
相关题目
10.下列粒子结构示意图中,表示阴离子的是( )
| A. | 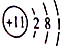 | B. | 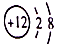 | C. | 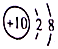 | D. | 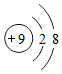 |
4.单晶硅是重要的半导体材料,某厂生产的单晶硅曾用于制造我国的第一颗人造卫星.在硅及相关产品的生产中排放的废水中含有HCI.该厂化验员对本厂排放废水中HCl的质量分数进行测定:将20mL废水(假定密度为1g/cm3)样品置于锥形瓶中,用质量分数为1%的氢氧化钠溶液进行中和,共用去氢氧化钠溶液8g(假设废水中不含其他能与氢氧化钠溶液反应的物质).
(1)计算该废水中含HCl的质量分数.
(2)他用了15克废牙膏皮(有效成分是铝),与上述20mL废水刚好反应,据此计算,废牙膏皮中铝的质量分数为多少?
(3)该厂每天产生废水100t,若直接排放将对环境造成污染,必须进行无害
化处理后才能进行排放,现准备用氢氧化钙粉末或氧化钙粉末进行中和.如下表所示:
你将选择CaO(写化学式)来中和废水中的HCl,请说明理由价格便宜.
(1)计算该废水中含HCl的质量分数.
(2)他用了15克废牙膏皮(有效成分是铝),与上述20mL废水刚好反应,据此计算,废牙膏皮中铝的质量分数为多少?
(3)该厂每天产生废水100t,若直接排放将对环境造成污染,必须进行无害
化处理后才能进行排放,现准备用氢氧化钙粉末或氧化钙粉末进行中和.如下表所示:
| 物 质 | 物质(或溶质)的相对分子质量 | 市场参考价(元/吨) |
| 氢氧化钙粉末 | 74 | 200 |
| 氧化钙粉末 | 56 | 150 |
11.溶质的质量分数为a%,密度为Pg/cm3的酒精浓溶液VmL,向其中加入xmL水稀释,则有关酒精稀溶液的计算不正确的是( )
| A. | 含溶质a•P•Vg | B. | 含溶剂$\frac{(100-a)•P•V}{100}+x$ | ||
| C. | 溶质的质量分数为$\frac{a•P•V}{P•V+x}$% | D. | 密度为$\frac{(PV+x)}{V+x}$g/cm3 |
13.实验室有三瓶失去标签的无色溶液,分别是稀盐酸、氢氧化钠溶液和氯化钠溶液中的一种,请你设计一个实验区分它们,完成实验报告.(提示:氯化钠溶液不能使石蕊溶液和酚酞溶液变色.)
| 操作 | 现象 | 结论 |
| 分别取少量样品于试管中,分别滴加紫色石蕊溶液 | 试管中溶液颜色分别显红色、蓝色、紫色 | 能使紫色石蕊溶液变红色的是稀盐酸,不变色的是氯化钠溶液,能使紫色石蕊溶液变蓝色的是氢氧化钠溶液 |
| 分别用pH试纸测定pH,与标准比色卡相比较 | 颜色分别显示红色、黄色、蓝色 | pH大于7的是氢氧化钠溶液,小于7的是稀盐酸,等于7的是氯化钠溶液 |
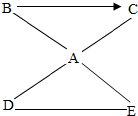 已知 A、B、C、D、E均为初中化学常见的物质,相互关系如图所示,“→”表示转化关系,“一”表示相互之间能反应(部分反应物、生成物以及反应条件省略).其中,A是人体胃酸的主要成分;B是一种常用的食品干燥剂,与水反应放出大量的热;C微溶于水;E是地壳中含量居第二位的金属元素.
已知 A、B、C、D、E均为初中化学常见的物质,相互关系如图所示,“→”表示转化关系,“一”表示相互之间能反应(部分反应物、生成物以及反应条件省略).其中,A是人体胃酸的主要成分;B是一种常用的食品干燥剂,与水反应放出大量的热;C微溶于水;E是地壳中含量居第二位的金属元素.