题目内容
20.生活中的下列现象,属于化学变化的是( )| A. | 玻璃破碎 | B. | 冰雪融化 | C. | 食物腐败 | D. | 衣服晾干 |
分析 本题考查学生对物理变化和化学变化的确定.判断一个变化是物理变化还是化学变化,要依据在变化过程中有没有生成其他物质,生成其他物质的是化学变化,没有生成其他物质的是物理变化.
解答 解:A、玻璃破碎只是形状的改变,属于物理变化,故A错;
B、冰雪融化只是状态的变化,没有新物质生成,属于物理变化,故B错;
C、食物腐败有菌类物质生成,属于化学变化,故C正确;
D、衣服晾干是水分蒸发的过程,没有新物质生成,属于物理变化,故D错.
故选C.
点评 搞清楚物理变化和化学变化的本质区别是解答本类习题的关键.判断的标准是看在变化中有没有生成其他物质.

练习册系列答案
相关题目
1.对下列各物质中的杂质检验或除去的方法不正确的是( )
| 物质 | 杂质 | 检验或除去的方法 | |
| A | NaCl | Na2CO3 | 用适量的硝酸钙除杂 |
| B | CaCO3 | CaO | 用无色的酚酞试液检验 |
| C | H2 | CO2 | 通过盛有氢氧化钠溶液的洗气瓶除杂 |
| D | CuO | Fe | 用稀硫酸除杂 |
| A. | A | B. | B | C. | C | D. | D |
8.金属材料在生产、生活中的应用非常广泛.
(1)吃火锅用的锅体是由铜合金制造的,主要是因为铜合金具有很好的B(填序号).
A.导电性 B.导热性 C.延展性
(2)金属锈蚀造成浪费.铁制品锈蚀的过程,实际上是铁与空气中的水和氧气发生化学反应的过程.
(3)目前世界上已有50%以上的废钢铁得到回收利用,其目的是A.
A.节约金属资源 B.合理开采矿物 C.防止钢铁生锈
(4)金属是一种重要的材料,人类的生活和生产都离不开金属.下表表示了金属活动性顺序表中铜、锡、铁和铝元素被人类大规模开发、利用的大致年限.
根据图1中数据和有关的化学知识,你认为金属大规模开发、利用的先后顺序跟下列③⑤有关.
①地壳中金属元素的含量;②金属的导电性;③金属的活动性;④金属的延展性;⑤金属冶炼的难易程度.
(5)实验室有锌片、铁片、铜片、稀硫酸、硫酸锌溶液、硫酸亚铁溶液和硫酸铜溶液7种物质,小红选择合适的物质,设计了以下三种方法对锌、铜、铁的金属活动性顺序进行验证.
①方法一所选用的3种物质是铁片、硫酸锌溶液和硫酸铜溶液.
②方法二所选用的3种物质是锌片、铜片和硫酸亚铁.
③方法三所选用4种物质是锌片、铁片、铜片和稀硫酸.
(6)炼铁的原理是利用一氧化碳与氧化铁反应,其反应的化学方程式为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2,在实验室里,可用图2所示装置进行实验:实验中玻璃管内的粉末由红色色变黑色,红色粉末氧化铁中的铁元素的化合价为+3价.
(7)某钢铁厂每天需消耗5 000t含Fe2O380%的赤铁矿石,该厂理论上可日产含Fe 98%的生铁2587.1t.(计算结果保留1位小数)
(8)某兴趣小组的同学对一批铁的样品(含有杂质,杂质不溶与水,也不与稀硫酸反应)进行分析,甲、乙、丙三位同学分别进行实验,其中一位同学所用的稀硫酸与铁样品恰好完全反应,实验数据如表:
请你认真分析数据,回答下列问题:
①乙同学所用的稀硫酸与铁的样品恰好完全反应?
②计算铁的样品中铁的质量分数.(写出详细的计算过程)
(1)吃火锅用的锅体是由铜合金制造的,主要是因为铜合金具有很好的B(填序号).
A.导电性 B.导热性 C.延展性
(2)金属锈蚀造成浪费.铁制品锈蚀的过程,实际上是铁与空气中的水和氧气发生化学反应的过程.
(3)目前世界上已有50%以上的废钢铁得到回收利用,其目的是A.
A.节约金属资源 B.合理开采矿物 C.防止钢铁生锈
(4)金属是一种重要的材料,人类的生活和生产都离不开金属.下表表示了金属活动性顺序表中铜、锡、铁和铝元素被人类大规模开发、利用的大致年限.

根据图1中数据和有关的化学知识,你认为金属大规模开发、利用的先后顺序跟下列③⑤有关.
①地壳中金属元素的含量;②金属的导电性;③金属的活动性;④金属的延展性;⑤金属冶炼的难易程度.
(5)实验室有锌片、铁片、铜片、稀硫酸、硫酸锌溶液、硫酸亚铁溶液和硫酸铜溶液7种物质,小红选择合适的物质,设计了以下三种方法对锌、铜、铁的金属活动性顺序进行验证.
①方法一所选用的3种物质是铁片、硫酸锌溶液和硫酸铜溶液.
②方法二所选用的3种物质是锌片、铜片和硫酸亚铁.
③方法三所选用4种物质是锌片、铁片、铜片和稀硫酸.
(6)炼铁的原理是利用一氧化碳与氧化铁反应,其反应的化学方程式为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2,在实验室里,可用图2所示装置进行实验:实验中玻璃管内的粉末由红色色变黑色,红色粉末氧化铁中的铁元素的化合价为+3价.
(7)某钢铁厂每天需消耗5 000t含Fe2O380%的赤铁矿石,该厂理论上可日产含Fe 98%的生铁2587.1t.(计算结果保留1位小数)
(8)某兴趣小组的同学对一批铁的样品(含有杂质,杂质不溶与水,也不与稀硫酸反应)进行分析,甲、乙、丙三位同学分别进行实验,其中一位同学所用的稀硫酸与铁样品恰好完全反应,实验数据如表:
| 甲 | 乙 | 丙 | |
| 烧杯+稀硫酸的质量 | 200 | 150 | 150 |
| 加入铁的样品的质量 | 9 | 9 | 14 |
| 充分反应后,烧杯+剩余物的质量 | 208.7 | 158.7 | 163.7 |
①乙同学所用的稀硫酸与铁的样品恰好完全反应?
②计算铁的样品中铁的质量分数.(写出详细的计算过程)
5.下列物品无论在水中,土壤中还是空气中都长久不能被分解或被腐蚀的是( )
| A. | 铁制品 | B. | 棉布 | C. | 常见塑料 | D. | 食品 |
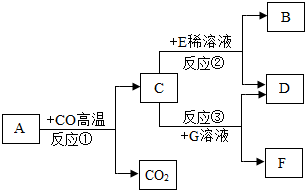 现有A~G七种物质,已知A是赤铁矿的主要成分,E的浓溶液有挥发性,G溶液为蓝绿色,它们之间存在如图所示的转化关系:
现有A~G七种物质,已知A是赤铁矿的主要成分,E的浓溶液有挥发性,G溶液为蓝绿色,它们之间存在如图所示的转化关系: