题目内容
11.某化学兴趣小组把一块比绿豆略大的金属钠,放入盛有20毫升硫酸铜溶液的烧杯中,发现金属钠浮在液面上不停打转,产生的气体燃烧并发出嘶嘶声,表层溶液中出现了蓝色絮状沉淀,絮状物慢慢下沉渐渐增多,并没有出现紫红色的铜.正准备整理器材,她们突然发现蓝色沉淀渐渐变黑.探究一:反应中生成的气体是什么?
【提出猜想】①欢欢认为该气体可能是氧气;②迎迎认为该气体可能是氢气.晶晶认为欢欢的假设是错误的.理由是氧气不可燃.
【查阅资料】钠与水反应生成氢氧化钠和氢气,该反应过程中放热(填“放热”或“吸热”).
【进行实验】晶晶在盛有蒸馏水的烧杯中先注入一些煤油,再投入金属钠,可以看到金属钠悬浮在煤油和水的界面上,并与水发生反应,将产生的气体收集检验,证明迎迎的猜想正确.金属钠悬浮在煤油和水的界面上,说明钠的密度小.
探究二:生成的黑色固体是什么物质?
【查阅资料】①硫酸铜与氢氧化钠反应生成氢氧化铜,该反应的化学方程式为:2NaOH+CuSO4═Cu(OH)2↓+Na2SO4;②氢氧化铜受热分解生成氧化铜和水.
小美猜想:黑色固体可能是氧化铜和铜的混合物.依据是量少而又细小的铜粉夹杂在氧化铜之间可能看不清.
【进行实验】为了进一步证实该黑色固体中是否含有铜,她们取少量该粉末放入试管,加入一定量的稀盐酸溶液,略微加热,发现固体全部消失,从而证实了小美的猜想不正确.
分析 探究一:【提出猜想】考虑氧气不可燃,而氢气可燃.
【查阅资料】根据实验现象“产生的气体燃烧并发出嘶嘶声,表层溶液中出现了蓝色絮状沉淀”,推测钠与水反应生成氢氧化钠和氢气为放热.
【进行实验】根据“金属钠悬浮在煤油和水的界面上”,说明钠的密度小.
探究二:【查阅资料】首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤进行书写即可.
【进行实验】考虑氧化铜与稀盐酸反应,进行分析.
解答 解:
探究一:【提出猜想】氧气不可燃,而氢气可燃,故晶晶认为欢欢的假设是错误的.
【查阅资料】根据实验现象“产生的气体燃烧并发出嘶嘶声,表层溶液中出现了蓝色絮状沉淀”,推测钠与水反应生成氢氧化钠和氢气为放热反应.
【进行实验】根据“金属钠悬浮在煤油和水的界面上”,说明钠的密度小.
探究二:
【查阅资料】氢氧化钠再和硫酸铜溶液反应,其反应的化学方程式为2NaOH+CuSO4═Cu(OH)2↓+Na2SO4.
【进行实验】为了进一步证实该黑色固体中是否含有铜,她们取少量该粉末放入试管,加入一定量的稀盐酸(稀硫酸或稀H2SO4 或稀HCl)溶液,略微加热,发现固体全部消失,从而证实了小美的猜想不正确.
故答案为:
探究一:
【提出猜想】氧气不可燃.【查阅资料】放热.【进行实验】小.
探究二:
【查阅资料】2NaOH+CuSO4═Cu(OH)2↓+Na2SO4.
【进行实验】稀盐酸(稀硫酸或稀H2SO4 或稀HCl).
点评 解读有用信息,对操作中的描述和反应现象认真加以分析,再结合自己所学知识,此类题可迎刃而解.

练习册系列答案
 挑战100单元检测试卷系列答案
挑战100单元检测试卷系列答案
相关题目
6.以下化学实验的基本操作正确的是( )
| A. | 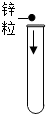 | B. | 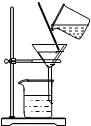 | C. | 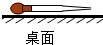 | D. | 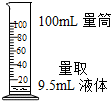 |
6.K2CO3和KNO3在不同温度时的溶解度及其溶解度曲线如下.
(1)图1中能表示KNO3溶解曲线的是甲(填“甲”或“乙”).
(2)曲线上M点的含义是t1℃时,KNO3和K2CO3的溶解度相同.
(3)40℃时,向两个分别盛有相同质量的硝酸钾和碳酸钾的烧杯中,各加入100g水,充分溶解后,恢复至40℃,其结果如图2所示.
下列有关说法中,正确的是C(填字母).
A、烧杯②中溶液是不饱和溶液
B、烧杯①中放的是碳酸钾
C、将得到的烧杯②中溶液降温至20℃时,溶液中溶质质量分数可能不变.

| 温度/℃ | 20 | 30 | 50 | 60 | 80 | |
| 溶解度/g | K2CO3 | 110 | 114 | 121 | 126 | 139 |
| KNO3 | 31.6 | 45.8 | 85.5 | 110 | 169 | |
(2)曲线上M点的含义是t1℃时,KNO3和K2CO3的溶解度相同.
(3)40℃时,向两个分别盛有相同质量的硝酸钾和碳酸钾的烧杯中,各加入100g水,充分溶解后,恢复至40℃,其结果如图2所示.
下列有关说法中,正确的是C(填字母).
A、烧杯②中溶液是不饱和溶液
B、烧杯①中放的是碳酸钾
C、将得到的烧杯②中溶液降温至20℃时,溶液中溶质质量分数可能不变.
3. 某组同学在学习盐的性质时,将碳酸钠溶液和一瓶标签破损的溶液M(如图)进行反应,有白色沉淀产生,过滤后得到澄清滤液.同学们对该实验进行了一系列的探究.
某组同学在学习盐的性质时,将碳酸钠溶液和一瓶标签破损的溶液M(如图)进行反应,有白色沉淀产生,过滤后得到澄清滤液.同学们对该实验进行了一系列的探究.
探究一:M溶液中的溶质是什么?
(1)【提出猜想】该组同学认为M溶液的溶质有两种可能:①是Ca(OH)2,②是CaCl2.
【收集资料】CaCl2水溶液呈中性.
(2)【设计实验】同学们设计了如下方案并进行实验:
请写出碳酸钠与溶液M反应的化学方程式Na2CO3+Ca(OH)2=CaCO3↓+2NaOH.
探究二 过滤后澄清滤液中会有哪些溶质?
【提出猜想】猜想一:NaOH 和Na2CO3;猜想二:NaOH和Ca(OH)2;猜想三:NaOH
(3)【实验验证】同学们针对“猜想一”进行了如下实验:
他们的实验结论是否正确?否,理由是加入的(少量)盐酸先与溶液中的氢氧化钠反应,即使溶液中有碳酸钠,也可能不产生气体.
(4)【继续探究】设计实验方案确定滤液中溶质的组成.
(5)【反思与拓展】在分析反应后所得溶液中溶质时,除考虑可溶性的生成物,还应考虑反应物是否有剩余.
 某组同学在学习盐的性质时,将碳酸钠溶液和一瓶标签破损的溶液M(如图)进行反应,有白色沉淀产生,过滤后得到澄清滤液.同学们对该实验进行了一系列的探究.
某组同学在学习盐的性质时,将碳酸钠溶液和一瓶标签破损的溶液M(如图)进行反应,有白色沉淀产生,过滤后得到澄清滤液.同学们对该实验进行了一系列的探究.探究一:M溶液中的溶质是什么?
(1)【提出猜想】该组同学认为M溶液的溶质有两种可能:①是Ca(OH)2,②是CaCl2.
【收集资料】CaCl2水溶液呈中性.
(2)【设计实验】同学们设计了如下方案并进行实验:
| 实验操作 | 实验现象 | 实验结论 |
| 取少量M溶液于试管中,向其中滴加无色酚酞试液 | 溶液变红色 | 猜想①正确. |
探究二 过滤后澄清滤液中会有哪些溶质?
【提出猜想】猜想一:NaOH 和Na2CO3;猜想二:NaOH和Ca(OH)2;猜想三:NaOH
(3)【实验验证】同学们针对“猜想一”进行了如下实验:
| 实验操作 | 实验现象 | 实验结论 |
| 取样于试管中,滴入几滴稀盐酸 | 没有气体产生 | “猜想一”不成立 |
(4)【继续探究】设计实验方案确定滤液中溶质的组成.
| 实验操作 | 实验现象 | 实验结论 |
| 分别取少量滤液于A、B两支试管中,A中加入CaCl2溶液, B中加入Na2CO3溶液 | 若A中产生白色沉淀,B中没有沉淀 | “猜想一”成立 |
| 若A中没有沉淀,B中产生白色沉淀 | “猜想二”成立 | |
| 若A、B两支试管中都没有沉淀产生 | “猜想三”成立 |
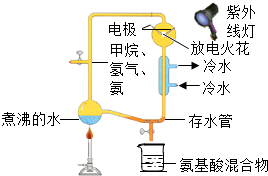 历史上巨行星(如木星和土星)的大气成分变化可能变小,而现在它们的大气中都没有游离氧,其主要成分是氢气、氦气、甲烷和氨.由此推断,原始地球空气成分和木星、土星上的大气成分类似.1953年米勒做了一个探索地球上的生命是如何起源的实验(如图是米勒实验的装置图).米勒向装置中通入推测的原始大气成分:甲烷、氢气、氨、水蒸气,通过放电和照射紫外线的方法代替原始地球的环境条件,获得了多种氨基酸.请根据右图回答下列问题:
历史上巨行星(如木星和土星)的大气成分变化可能变小,而现在它们的大气中都没有游离氧,其主要成分是氢气、氦气、甲烷和氨.由此推断,原始地球空气成分和木星、土星上的大气成分类似.1953年米勒做了一个探索地球上的生命是如何起源的实验(如图是米勒实验的装置图).米勒向装置中通入推测的原始大气成分:甲烷、氢气、氨、水蒸气,通过放电和照射紫外线的方法代替原始地球的环境条件,获得了多种氨基酸.请根据右图回答下列问题: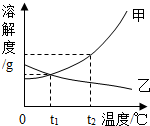 如图是甲、乙两种固体物质的溶解度曲线.
如图是甲、乙两种固体物质的溶解度曲线.