题目内容
12.工业上用煅烧石灰石(主要成分为CaCO3)制取生石灰(主要成分CaO),同时得到二氧化碳.(1)某工厂用500t含杂质10%(杂质不分解)的石灰石,其中所含碳酸钙的质量是450t.
(2)上述石灰石理论上可以制得生石灰多少?
分析 (1)根据石灰石的质量、杂质的质量分数可以计算碳酸钙的质量;
(2)根据碳酸钙的质量可以计算生成氧化钙的质量.
解答 解:(1)该石灰石所含碳酸钙质量为:500t×(1-10%)=450t.
(2)设生成氧化钙的质量为x
CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑
100 56
450t x
$\frac{100}{450t}$=$\frac{56}{x}$
解得:x=252t
答:石灰石理论上可以制得生石灰252t.
故答案为:(1)450t;
(2)252t.
点评 本题难度不大,掌握根据化学方程式的计算即可正确解答本题,解题时要注意解题的规范性.

练习册系列答案
 华东师大版一课一练系列答案
华东师大版一课一练系列答案
相关题目
14.下列变化中,属于物理变化的是( )
| A. | 牛奶变酸 | B. | 煤气中毒 | C. | 钢铁生锈 | D. | 酒精挥发 |
20.下列说法,正确的是( )
| A. | 在面粉中加入适量的水,充分搅拌,可得到溶液 | |
| B. | 饱和溶液一定比不饱和溶液的浓度大 | |
| C. | 洗涤清可洗去餐具上的油污,是因为洗涤清具有乳化功能 | |
| D. | 只用水作试剂不能将氯化钠、氢氧化钠、硝酸铵三种物质区分开来 |
4.下列物质放入水中能形成溶液且温度降低的是( )
| A. | 面粉 | B. | 冰块 | C. | 蔗糖 | D. | 硝酸铵 |
2.下列说法正确的是( )
| A. | 空气中氧气的体积分数最大 | |
| B. | 原子的质量几乎都集中在原子核中 | |
| C. | 人体中含量较多的前四种元素是碳、氧、氢、氮 | |
| D. | 由不同种元素组成的物质一定是混合物 |

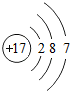 原子序数为17的氯元素的原子结构示意图如图所示,该原子在化学反应中易得到(填“得到”或“失去”)电子,形成阴离子(填“阴离子”或“阳离子”).
原子序数为17的氯元素的原子结构示意图如图所示,该原子在化学反应中易得到(填“得到”或“失去”)电子,形成阴离子(填“阴离子”或“阳离子”).