题目内容
4.随着经济的发展,能源与环境成为人们日益关注的问题.(1)燃煤发电时,将煤块粉碎成煤粉,其目的是增大与氧气的接触面积,使燃烧更充分.
(2)化石燃料燃烧都会产生二氧化碳,它是空气中含量最多的温室气体.为减少它的排放,科学家致力于研究将过多的二氧化碳和氢气在催化剂和加热的条件下反应,转化为水和甲烷.该反应的化学方程式为CO2+4H2$\frac{\underline{\;催化剂\;}}{△}$CH4+2H2O.
(3)“绿色化学”的特点之一是“零排放”.一定条件下,二氧化碳和氢气可以按照不同比例反应,生成下列有机物.其中二氧化碳和氢气反应,只生成一种产物就能实现“零排放”,这种产物是B(填字母序号,下同).
A.甲醇(CH4O) B.甲酸(CH2O2) C.乙醇(C2H6O) D.乙酸(C2H4O2)
(4)下列做法中不符合“低碳经济”理念的是(填序号)②⑤;
①改造或淘汰高能耗、高污染产业;②大力发展火力发电;
③研制和开发新能源替代传统能源;
④优化建筑设计,增强室内自然采光,减少照明用电;
⑤禁止使用煤、石油、天然气等矿物燃料
(5)请你另举一例在日常生活中你能做到符合“节能减排”的做法双面使用纸、随手关灯等.
分析 (1)根据燃料的条件及使燃烧更充分的方法进行分析;
(2)根据反应物、生成物及质量守恒定律书写化学方程式;
(3)根据“二氧化碳和氢气反应,只生成一种产物”可判断所生成的有机物中C、O元素的原子个数比应与CO2中C、O元素的原子个数相同为1:2;根据所生成有机物中C、O元素的原子个数比,判断四个选项中符合此特点的化学式即该物质的化学式.
(4)可以根据“低碳经济”的含义方面进行分析、判断,从而得出正确的结论.
(5)根据日常生活中你能做到符合“节能减排”的措施回答,要注意是日常生活中的例子,是个人能做到的.
解答 解:(1)燃煤发电时,将煤块粉碎成煤粉,其目的是增大与氧气的接触面积,使燃烧更充分,故答案为:增大与氧气的接触面积,使燃烧更充分;
(2)二氧化碳和氢气在催化剂、加热的条件下转化为水和甲烷,该反应的化学方程式为:CO2+4H2$\frac{\underline{\;催化剂\;}}{△}$CH4+2H2O;故答案为:CO2+4H2$\frac{\underline{\;催化剂\;}}{△}$CH4+2H2O;
(3)A、根据化学式CH4O,可知该物质中C、O元素的原子个数比为1:1,不符合所生成有机物的特点,故A错误;
B、根据化学式CH2O2,可知该物质中C、O元素的原子个数比为1:2,符合所生成有机物的特点,故B正确;
C、根据化学式C2H6O,可知该物质中C、O元素的原子个数比为2:1,不符合所生成有机物的特点,故C错误;
D、根据化学式C2H4O2,可知该物质中C、O元素的原子个数比为1:1,不符合所生成有机物的特点,故D错误.
故选B.
(4)改造或淘汰高能耗、高污染产业符合“低碳经济”的理念.大力发展火力(用煤作燃料)发电能生成大量的污染环境的物质,不符合“低碳经济”的理念.
研制和开发新能源替代传统能源符合“低碳经济”的理念.优化建筑设计,增强室内自然采光,减少照明用电符合“低碳经济”的理念;禁止使用煤、石油、天然气不合理,因为这三种物质是重要的化工原料;故填:②⑤;
(5)“节能减排”从我做起,如随手关灯,或步行代替乘车,或纸双面用等,故填:双面使用纸、随手关灯等.
点评 解答本题的关键是要掌握“低碳经济”的含义方面的知识,只有这样才能对问题做出正确的判断.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案探究Ⅰ:证明氢氧化钠溶液与稀盐酸确实能发生反应.
【方案1】测定稀盐酸与NaOH溶液混合前后的pH.
测定某NaOH溶液的pH,pH大于7.将一定量的稀盐酸加入该NaOH溶液中,混合均匀后测定其pH,发现pH减小了,但仍然大于7,小组中有的同学认为根据这个测定结果可以认为稀盐酸与NaOH溶液发生了反应,你认为他们的结论是否正确:不正确,理由氢氧化钠溶液中加水稀释pH也会减小.经过讨论后,他们向溶液中又加入一定量的稀盐酸,混合均匀后测定其pH,pH 小于7.
结论:稀盐酸与氢氧化钠溶液发生了化学反应,并且稀盐酸过量.
【方案2】借助于无色酚酞试液.
【药品仪器】如图1
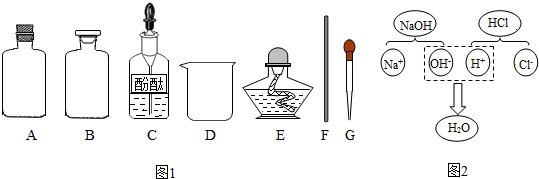
①取A(选填“A”或“B”)中试剂加入至D中,滴加2滴酚酞试液,溶液呈红色;
②用胶头滴管向①中溶液滴加稀盐酸,红色消失;
③用F蘸取②中溶液,在酒精灯上灼烧,有白色固体产生.
【思考拓展】
(1)如不使用酸碱指示剂,进一步确认步骤③中的白色固体不是氢氧化钠的方法是:取少量水将其溶解加入CuSO4溶液,无蓝色沉淀.
(2)探究步骤②中无色溶液中稀盐酸是否过量.
根据上述反应过程中溶液变成无色,不能确定稀盐酸是否过量,兴趣小组同学又分别选取了AgNO3溶液、紫色石蕊试液、Na2CO3粉末设计实验方案,请你分析并判断:
| 实验方案 | 实验步骤 | 现 象 | 结 论 |
| ① | 取样,加入适量的AgNO3溶液 | 出现白色沉淀 | 稀盐酸过量 |
| ② | 取样,加入几滴紫色石蕊试液 | 溶液变红 | 稀盐酸过量 |
| ③ | 取样,加入铁锈粉末 | 红棕色粉末逐渐减少,溶液变成黄色 | 稀盐酸过量 |
请你再设计一个与上述实验不同原理的方案以确定稀盐酸是否过量,你选用的试剂是Na2CO3溶液或锌等.
(3)不是所有的碱与盐酸反应都无明显现象,例如Cu(OH)2(填一种碱)与盐酸反应就有明显的实验现象.
探究Ⅱ:从微观的角度认识物质及其变化的本质.图2表示氢氧化钠溶液与盐酸反应的微观过程,该反应的本质是氢离子和氢氧根离子;结合生成水.请写出一个与上述反应本质相同的化学方程式:2NaOH+H2SO4=Na2SO4+2H2O.
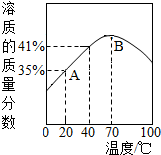 ZnSO4饱和溶液的溶质质量分数随温度变化的曲线如图所示.下列说法正确的是( )
ZnSO4饱和溶液的溶质质量分数随温度变化的曲线如图所示.下列说法正确的是( )| A. | ZnSO4饱和溶液的溶质质量分数随温度升高而增大 | |
| B. | 点A对应的ZnSO4溶液是不饱和溶液 | |
| C. | 点B对应的ZnSO4溶液升温或降温均能达到饱和 | |
| D. | 40℃时,ZnSO4的溶解度为41g |

 化学来源于生活,应用于生活,化学与我们的日常生活密切相关.
化学来源于生活,应用于生活,化学与我们的日常生活密切相关.