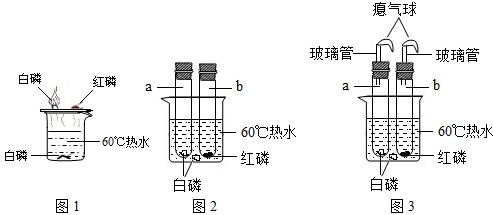
题目内容
20.黄色固体粉末A在空气中燃烧,发出微弱的淡蓝色火焰,而在B物质中可以剧烈燃烧,发出明亮的蓝紫色火焰,生成有刺激性气味的气体C.黑色粉末D和白色晶体E共热反应生成B和F,且在反应前后D的质量不变.(1)试推断A、B、C、D、E、F各是什么物质?(分别写出它们的名称):
A硫 B氧气C二氧化硫 D二氧化锰E氯酸钾 F氯化钾
(2)写出A在B中燃烧的文字表达式及基本反应类型:硫+氧气$\stackrel{点燃}{→}$二氧化硫(化合反应);
(3)写出D和E共热的文字表达式及反应类型:氯酸钾$\underset{\stackrel{二氧化锰}{\overrightarrow{加热}}}{\;}$氯化钾+氧气(分解反应).
分析 本题的突破口是物质的颜色和特殊的化学化学反应.根据“黄色固体粉末A在空气中燃烧,发出微弱的淡蓝色火焰,而在B物质中可以剧烈燃烧,发出明亮的蓝紫色火焰,生成有刺激性气味的气体C”,则叙述情况和硫在氧气燃烧情况一致,硫是淡黄色固体粉末,二氧化硫气体有刺激性气味,说明A是硫,B是氧气,C是二氧化硫;根据“黑色粉末D和白色晶体E共热反应生成B和F,且在反应前后D的质量不变”,叙述情况和氯酸钾在二氧化锰的催化下制氧气的情况一致,说明E是氯酸钾,D是二氧化锰,B是氧气,F是氯化钾.
解答 解根据“黄色固体粉末A在空气中燃烧,发出微弱的淡蓝色火焰,而在B物质中可以剧烈燃烧,发出明亮的蓝紫色火焰,生成有刺激性气味的气体C”,则叙述情况和硫在氧气燃烧情况一致,硫是淡黄色固体粉末,二氧化硫气体有刺激性气味,说明A是硫,B是氧气,C是二氧化硫;根据“黑色粉末D和白色晶体E共热反应生成B和F,且在反应前后D的质量不变”,叙述情况和氯酸钾在二氧化锰的催化下制氧气的情况一致,说明E是氯酸钾,D是二氧化锰,B是氧气,F是氯化钾.
硫和氧气在点燃的条件下生成二氧化硫,故答案为:硫+氧气$\stackrel{点燃}{→}$二氧化硫,为化合反应.
氯酸钾在二氧化锰的催化作用下加热会生成氯化钾和氧气,故答案为:氯酸钾$\underset{\stackrel{二氧化锰}{\overrightarrow{加热}}}{\;}$氯化钾+氧气,为分解反应;
故答案为:
(1)硫; 氧气;二氧化硫;二氧化锰;氯酸钾;氯化钾
(2)硫+氧气$\stackrel{点燃}{→}$二氧化硫( 化合反应);
(3)氯酸钾$\underset{\stackrel{二氧化锰}{\overrightarrow{加热}}}{\;}$氯化钾+氧气( 分解反应).
点评 推断题的关键是突破口的选择,颜色,重要的反应都可以作为突破口,同时要敢于尝试,记住重要的化学反应和一些特殊物质的颜色.

| A. | 6 2 | B. | 4 6 | C. | 5 5 | D. | 2 8 |
| A. |  向一定量的稀硫酸溶液中逐滴加入氢氧化钡溶液 | |
| B. |  将浓盐酸敞口放置在空气中 | |
| C. | 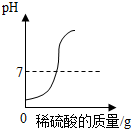 向一定质量的氢氧化钠溶液中不断滴加稀硫酸 | |
| D. | 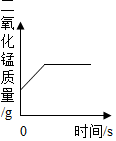 加热氯酸钾和二氧化锰的固体混合物 |
| 实验操作 | 实验现象 | 实验结论 | 总结 | |
| 实验一 | 取5ml 5%过氧化氢溶液于试管中,伸入带火星的木条 | 有气泡产生,木条不复燃 | 过氧化氢分解产生氧气,但是反应慢.反应的化学方程式为:2H2O2═2H2O+O2↑ | 二氧化锰是过氧化氢分解的催化剂 |
| 实验二 | 向盛水的试管中加入二氧化锰,伸入带火星的木条 | 没有明显现象 | 二氧化锰加入水中不产生氧气 | |
| 实验三 | 向盛有5mL5%过氧化氢溶液的试管中加入二氧化锰,伸入带火星的木条 | 有大量气泡产生,带火星的木条迅速复燃 | 二氧化锰能加快过氧化氢的分解 |
(2)写出实验三中化学反应的符号表达式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑:
(3)小英同学认为仅由上述实验还不能完全表内的“总结”,她补充设计了两个方面的探究实验,最终完成了对“命题”的实验证明.
第一方面的实验操作中包含了两次称量,其目的是:比较MnO2在过氧化氢分解前后的质量;
第二方面的实验是利用“实验三”反应后试管内的剩余物继续实验.接下来的实验操作是:倾倒掉反应后的液体,向剩余的固体中重新加入过氧化氢溶液,有大量气泡产生,说明MnO2仍然能加快过氧化氢的分解速率(化学性质没变).
| A. | 海洋 | B. | 江河 | C. | 湖泊 | D. | 地下水 |