题目内容
1.某化学课外小组同学,用如图所示实验验证质量守恒定律.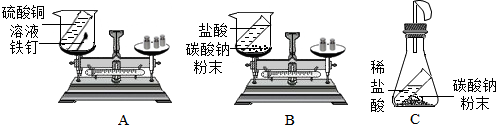
(1)某甲同学用A装置探究质量守恒定律,实验步骤如下:
如图将烧杯放在天平上用砝码平衡,然后倾斜烧杯使硫酸铜溶液与铁钉接触,一段时间后再把烧杯放在天平上.
①发生反应的化学方程式为Fe+CuSO4═FeSO4+Cu.
②最后天平的指针(填序号)C(a.偏左 b.偏右 c.不偏转 d.无法预测).
(2)乙同学用B装置研究质量守恒定律,实验步骤如下:
如图将烧杯放在天平上用砝码平衡,然后倾斜烧杯使盐酸与碳酸钠粉末接触,一段时间后再把烧杯放在天平上.发现天平的指针偏右.
①造成天平的指针向右偏转的原因是盐酸与碳酸钠粉末反应的装置不密闭,生成二氧化碳气体逸出,使左盘内质量减小.
②若将本实验中的烧杯替换成带有气球的锥形瓶,如图C所示,其他操作不变,最后天平仍不平衡.
可见,在验证质量守恒定律时,若利用有气体参加或有气体生成的化学反应来设计实验,在装置设计方面应做到装置密闭,体积不变.
(3)在化学反应前后,一定不变的是(填序号)①②③⑥.
①元素种类 ②原子种类 ③原子数目
④分子种类 ⑤分子数目 ⑥物质的总质量
(4)红热的铁能与水蒸气反应,放出气体X,同时生成固体Y.X气体靠近火焰点火时,能燃烧或发出爆鸣声.其反应的化学方程式为:3Fe+4H2O$\frac{\underline{\;\;△\;\;}}{\;}$ 4X+Y.则X的化学式为H2,Y的化学式为Fe3O4.
(5)应用质量守恒定律可以确定反应物或产物的化学式.在载人宇宙飞船中,一般都安装盛放过氧化钠(Na2O2)颗粒的装置,它的作用是再生氧气,供宇航员呼吸,反应的化学方程式为2Na2O2+2CO2═2X+O2.则X的化学式为Na2CO3.
(6)镁是一种很活泼的金属,点燃后,它既能在氮气中燃烧也能在二氧化碳中燃烧.已知镁在氮气中燃烧化合成一种物质,其中氮元素的化合价为-3价.试写出此反应的化学方程式:3Mg+N2$\frac{\underline{\;点燃\;}}{\;}$Mg3N2.
分析 (1)根据硫酸铜溶液与铁钉反应生成硫酸亚铁和铜,写出反应的方程式解答;
(2)根据用实验来验证质量守恒定律,那么结果不外乎两个:相等(当没有气体参加或不生成气体时)、不相等 (当有气体参加或生成气体时)解答;
(3)考查的是质量守恒定律的守恒原因,根据宏观方面的以及微观方面的解答.
(4)根据质量守恒定律,原子的种类和原子的数目均不变.数一数原子的数目,看一看元素的种类,你会判断出X、Y的化学式;
(5)用质量守恒定律解决一些常见类型的题目,主要利用守恒的原因来解答;
(6)由题目所给信息不难写出反应的化学方程式;注意书写化学方程式的两原则:一、尊重事实;二遵守质量守恒定律.
解答 解:(1)①硫酸铜溶液与铁钉反应生成硫酸亚铁和铜,烧杯内反应的实验现象为铁钉表面出现红色的固体,溶液有蓝色变为浅绿色,故反应的方程式为:Fe+CuSO4═FeSO4+Cu;
②甲同学所做的实验中,没有气体参加或生成,所以左右肯定平衡,故选C;
(2)①乙同学所做的实验中,有气体二氧化碳生成,故造成天平的指针向右偏转的原因是:盐酸与碳酸钠粉末反应的装置不密闭,生成二氧化碳气体逸出,使左盘内质量减小;
②要想使两边相等,只能把生成的气体收集起来,不让其出去,也就是说必须在密闭容器中进行了;但本实验中的烧杯替换成带有气球的锥形瓶,最后天平仍不平衡.原因是:反应产生的二氧化碳是气球膨胀,因此装置受到的浮力会增大;
可见,在探究质量守恒定律时,若利用有气体参加或有气体生成的化学反应来设计实验,在装置设计方面应做到:装置密闭,体积不变;
故答案为:盐酸与碳酸钠粉末反应的装置不密闭,生成二氧化碳气体逸出,使左盘内质量减小;装置密闭,体积不变;
(3)质量守恒的原因:宏观是因为物质的总质量不变、元素的种类、元素的质量;微观是因为:原子的种类、原子的数目、原子的质量不变,故在化学反应前后,一定不变的是①②③⑥;
(4)X气体能燃烧并发出爆鸣声,根据元素种类不变,可知是氢气.根据反应前后原子的种类和个数不变,可得出Y的化学式为Fe3O4.
(5)根据反应前后元素的种类不变,可知X中含Na、C、O元素.根据反应前后原子的数目不变,可知X的化学式为Na2CO3
(6)由题目所给信息,镁在氮气中燃烧生成的氮化镁,可以看出反应物是镁和氮气,生成物是氮化镁;由氮元素的化合价可以写出氮化镁的化学式,进而写出反应的化学方程式:
3Mg+N2$\frac{\underline{\;点燃\;}}{\;}$Mg3N2
答案:
(1)①Fe+CuSO4═FeSO4+Cu;②c
(2)①盐酸与碳酸钠粉末反应的装置不密闭,生成二氧化碳气体逸出,使左盘内质量减小;
②装置密闭,体积不变;
(3)①②③⑥.
(4)H2;Fe3O4
(5)Na2CO3
(6)3Mg+N2$\frac{\underline{\;点燃\;}}{\;}$Mg3N2.
点评 本题考查的是质量守恒定律的运用,理解微观上质量守恒的原因、注意反应物或生成物中气体易被忽略等是正确解答本题的关键.

 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案
| A. | 加热前应检查装置的气密性 | |
| B. | 试管①与试管③中的水分子结构不同 | |
| C. | 导管②中主要发生水三态变化中的液化过程 | |
| D. | 试管①中溶质的质量分数越来越大 |
【问题1】铁燃烧时溅落下来的黑色物质中还有没有铁呢?
【查阅资料1】
(1)自然界中铁的氧化物主要是Fe3O4和Fe2O3两种(FeO极易被氧化为Fe2O3);
(2)铁的氧化物均能溶于酸的溶液.
【实验探究】将冷却后的黑色物质碾碎,装入试管,加入稀盐酸溶液,观察到的现象是冒气泡,说明铁燃烧时溅落下来的黑色物质中还含有铁.
| Fe3O4 | Fe2O3 | 铁 | |
| 分解温度/℃ | 1538 | 1400 | - |
| 熔点/℃ | - | - | 1535 |
【查阅资料2】
(1)Fe3O4和Fe2O3的分解温度、铁的熔点见表:
(2)Fe2O3高温时分解成Fe3O4.
【理论探讨】
结合表中数据,可推知铁在氧气里燃烧时产生的高温应在l535℃~l538℃之间,在此温度范围内Fe2O3已分解,所以铁在氧气里燃烧的产物是Fe3O4.
【拓展延伸】
(1)实验中为了防止集气瓶炸裂,必须在集气瓶底部放少量的水(或在集气瓶底部铺一层细沙);
(2)有些食品包装盒的透明盖内放有黑色的FeO粉末,若粉末的颜色由黑色变成红色,就说明包装盒破损进气,这样售货员就能及时发现并处理.
(3)下列铁的氧化物中,铁元素的质量分数由大到小的顺序是A>C>B(填字母).
A.FeO B.Fe2O3C.Fe3O4.
| A. | 反应产生的气体都有毒 | B. | 反应的生成物不同 | ||
| C. | 反应类型都是置换反应 | D. | 反应中都有红色固体生成 |
 溶解度曲线:甲、乙、丙三种固体物质的溶解度曲线如右图所示,下列有关说法中正确的是
溶解度曲线:甲、乙、丙三种固体物质的溶解度曲线如右图所示,下列有关说法中正确的是
 小明同学在实验室里加热混有二氧化锰的氯酸钾(KClO3)固体制氧气的装置如右图所示. 试回答下列问题:
小明同学在实验室里加热混有二氧化锰的氯酸钾(KClO3)固体制氧气的装置如右图所示. 试回答下列问题: