题目内容
4.铁的使用非常广泛,但较容易生锈.(1)工业上炼铁的反应原理是:O+Fe2O3=2Fe+3CO2,该反应中一氧化碳(CO)会夺取氧化铁(Fe2O3)中的氧,这说明一氧化碳具有还原性.
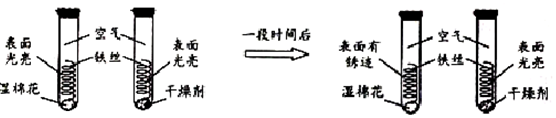
(2)根据下图所示实验现象,可以得出铁生锈的条件之一是水(或H2O).
分析 (1)根据在反应中,氧化铁失去了氧,发生了还原反应,是氧化剂.表现了氧化性,一氧化碳得到了氧,发生了氧化反应,是还原剂,表现了还原性进行解答;
(2)根据铁生锈的主要条件是铁与水和空气直接接触以及控制变量的方法进行解答.
解答 解:(1)在反应中,氧化铁失去了氧,发生了还原反应,是氧化剂.表现了氧化性,一氧化碳得到了氧,发生了氧化反应,是还原剂,表现了还原化性;故填:还原;
(2)铁生锈的主要条件是铁与水和空气直接接触,二者的不同之处是湿棉花可以提供水分,干燥剂不能提供水分,所以得出铁生锈的条件之一是水.故填:水.
故答案为:(1)还原;(2)水(或H2O).
点评 解答本题的关键是要充分理解氧化还原反应的含义,知道氧化剂在反应中提供了氧的特征,只有这样才能对问题做出正确的判断.

练习册系列答案
相关题目
14.化学实验活动课上,同学们利用如图实验探究氢氧化钙的性质.
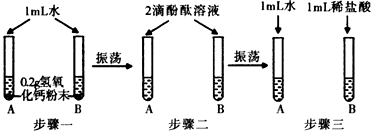
(1)上述三个步骤的A试管中的固体始终无明显减少,那么能说明A试管的水中溶有氢氧化钙的现象是步骤二中A中的溶液变红色.
(2)以上实验结束后,B试管中的固体消失,溶液澄清并呈无色.
【提出问题】步骤三B试管的溶液中,除指示剂外,溶质的成分还有什么?
【猜想】猜想一:CaCl2、HCl 猜想二:CaCl2、Ca(OH)2、HCl 猜想三:CaCl2
【小组讨论】同学们经过讨论得出猜想二一定是错误的.
【实验探究】小红同学利用了下面的实验验证了猜想一.
写出加入锌粒后发生反应的化学方程式Zn+2HCl═ZnCl2+H2↑.
【讨论交流】小红同学所做的实验结束后,试管中所得溶液一定含有的溶质是氯化钙、氯化锌(除指示剂外)

(1)上述三个步骤的A试管中的固体始终无明显减少,那么能说明A试管的水中溶有氢氧化钙的现象是步骤二中A中的溶液变红色.
(2)以上实验结束后,B试管中的固体消失,溶液澄清并呈无色.
【提出问题】步骤三B试管的溶液中,除指示剂外,溶质的成分还有什么?
【猜想】猜想一:CaCl2、HCl 猜想二:CaCl2、Ca(OH)2、HCl 猜想三:CaCl2
【小组讨论】同学们经过讨论得出猜想二一定是错误的.
【实验探究】小红同学利用了下面的实验验证了猜想一.
| 实验操作 | 实验现象 | 实验结论 |
| 取步骤三B试管中溶液样品倒入盛有锌粒的试管中 | 产生气泡 | 猜想一正确 |
【讨论交流】小红同学所做的实验结束后,试管中所得溶液一定含有的溶质是氯化钙、氯化锌(除指示剂外)
12.超音速飞机所排放的NO、NO2可与臭氧层中的臭氧(O3)和氧原子(O)发生下列反应,而使臭氧层遭到破坏.NO+O3=NO2+O2 NO2+O=NO+O2
那么,NO在破坏臭氧层的反应中所起的作用是( )
那么,NO在破坏臭氧层的反应中所起的作用是( )
| A. | 氧化 | B. | 还原 | C. | 催化 | D. | 分解 |
9.某无色气体可能含有H2、CO、CH4中的一种或几种,依次进行下列实验(假设每一步反应或吸收均完全):①无色气体在氧气中充分燃烧;②燃烧生成的气体通过盛浓硫酸的洗气瓶,装置质量增加10.8g;③再将剩余气体通过盛NaOH溶液的洗气瓶,装置质量增加13.2g.下列推断正确的是( )
| A. | 该气体可能含有CH4和H2 | B. | 该气体一定含有H2和CO | ||
| C. | 该气体可能含有CO和CH4 | D. | 该气体可能含有H2、CO、CH4 |
14.甲乙是某同学设计的两套制取二氧化碳的发生装置,对两套装置分析不正确的是( )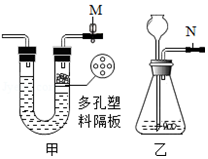

| A. | 此时甲装置中的止水夹M处于关闭状态 | |
| B. | 甲装置气体导出过程中容器内外气压相等 | |
| C. | 甲装置具有控制反应进行与否的功能 | |
| D. | 乙装置N处添加止水夹可以与甲装置具有相同功能 |
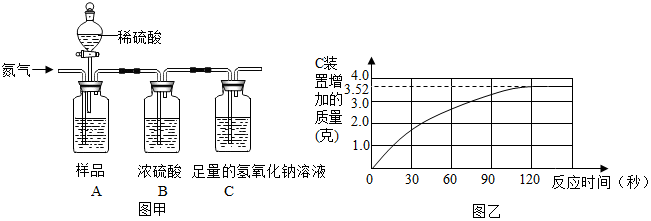
 如图是某试剂瓶标签的部分内容.请回答下列问题:
如图是某试剂瓶标签的部分内容.请回答下列问题: