题目内容
15.氢氧化钠是一种常见的碱.(1)氢氧化钠俗名叫烧碱(填一个).它具有强烈的腐蚀性,如果不慎沾到皮肤上,要用大量的水冲洗,再涂上硼酸溶液.
(2)氢氧化钠曝露在空气中容易吸收水分,表面潮湿并逐渐溶解,这种现象叫做潮解.
(3)电解水实验中,水中可加入少量氢氧化钠以增强导电性,这是因为氢氧化钠在水中会解离出Na+、OH-(填离子符号),随着水的分解,溶液的pH会增大(填“增大”或“减小”).
(4)10g一定溶质质量分数的氢氧化钠溶液与5g质量分数为9.8%的稀硫酸恰好完全反应.试计算该氢氧化钠溶液中溶质的质量分数.
分析 (1)根据氢氧化钠俗名叫烧碱、火碱、苛性钠,氢氧化钠具有强烈的腐蚀性,如果不慎沾到皮肤上,要用大量的水冲洗,再涂上硼酸溶液;
(2)根据氢氧化钠曝露在空气中容易吸收水分,表面潮湿并逐渐溶解的现象叫做潮解进行分析;
(3)根据氢氧化钠在水中会电离出钠离子、氢氧根离子,随着水的分解,氢氧化钠的浓度增大,所以溶液的pH会增大进行分析;
(4)根据氢氧化钠和硫酸反应的化学方程式和题中的数据进行计算.
解答 解:(1)氢氧化钠俗名叫烧碱、火碱、苛性钠,氢氧化钠具有强烈的腐蚀性,如果不慎沾到皮肤上,要用大量的水冲洗,再涂上硼酸溶液;
(2)氢氧化钠曝露在空气中容易吸收水分,表面潮湿并逐渐溶解的现象叫做潮解;
(3)氢氧化钠在水中会电离出Na+、OH-,随着水的分解,氢氧化钠的浓度增大,所以溶液的pH会增大;
(4)稀硫酸中溶质的质量为:5g×9.8%=0.49g
设该氢氧化钠溶液中溶质的质量为x
2NaOH+H2SO4=Na2SO4+2H2O
80 98
x 0.49g
$\frac{80}{x}$=$\frac{98}{0.49g}$
x=0.4g
该氢氧化钠溶液中溶质的质量分数为$\frac{0.4g}{10g}$×100%=4%.
故答案为:(1)烧碱,水;
(2)潮解;
(3)Na+、OH-,增大;
(4)该氢氧化钠溶液中溶质的质量分数为4%.
点评 本题主要考查了氢氧化钠的有关性质和化学方程式的计算,难度不大,注意在平时加强训练即可完成.

练习册系列答案
 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案
相关题目
5.日前科学家发现了一种新型二维半导体材料一氧化锡(SnO),该发现有望将电子设备速度提高100倍.下列关于一氧化锡的说法正确的是( )
| A. | 它是混合物 | |
| B. | 它的分子静止不动 | |
| C. | 它的分子之间不再有间隔 | |
| D. | 它的一个分子由1个氧原子和1个锡原子构成 |
5.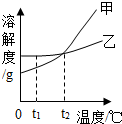 分析处理图表中的信息是学习化学的一种重要方法,运用溶解度表与溶解度曲线回答下列问题:
分析处理图表中的信息是学习化学的一种重要方法,运用溶解度表与溶解度曲线回答下列问题:
(1)氯化钠的溶解度曲线是乙(填“甲”或“乙”).
(2)20℃时,将40gNH4Cl加入100g的水中,充分搅拌后得到的是饱和溶液(填“饱和”或“不饱和”),将上述溶液升温到30℃,该溶液的溶质质量分数为$\frac{40g}{40g+100g}$×100%(只列计算式,不需计算结果).
(3)如图,t1℃时,将两种物质的饱和溶液各100g,分别恒温蒸发5g水,析出晶体最多的是乙(填“甲”或“乙”).
(4)计算配制50g质量分数为3%的NaCl溶液所需要质量分数为6%的NaCl溶液的体积,需要用到的数据是C.
A.3%的NaCl溶液的密度 B.水的密度 C.6%的NaCl溶液的密度.
 分析处理图表中的信息是学习化学的一种重要方法,运用溶解度表与溶解度曲线回答下列问题:
分析处理图表中的信息是学习化学的一种重要方法,运用溶解度表与溶解度曲线回答下列问题:| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 |
| NaCl溶解度/g | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 |
| NaCl溶解度/g | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 |
(2)20℃时,将40gNH4Cl加入100g的水中,充分搅拌后得到的是饱和溶液(填“饱和”或“不饱和”),将上述溶液升温到30℃,该溶液的溶质质量分数为$\frac{40g}{40g+100g}$×100%(只列计算式,不需计算结果).
(3)如图,t1℃时,将两种物质的饱和溶液各100g,分别恒温蒸发5g水,析出晶体最多的是乙(填“甲”或“乙”).
(4)计算配制50g质量分数为3%的NaCl溶液所需要质量分数为6%的NaCl溶液的体积,需要用到的数据是C.
A.3%的NaCl溶液的密度 B.水的密度 C.6%的NaCl溶液的密度.
6.今年3月26日是本年度的“地球一小时”(Earth Hour)活动日,目的是号召公众从衣食住行做起,践行可持续的生活和消费方式.作为一名中学生,你认为下列做法不应该提倡的是( )
| A. | 拒绝使用一次性木筷 | B. | 露天焚烧秸秆 | ||
| C. | 多骑自行车和乘公交车 | D. | 减少空调的使用 |
10.在含有大量H+、Na+、SO42-的溶液中,还可能大量存在的是( )
| A. | NH4+ | B. | Ba2+ | C. | OH- | D. | HCO3- |
4.拉瓦锡研究空气成分时涉及到的反应为2HgO$\frac{\underline{\;\;△\;\;}}{\;}$2Hg+O2↑,该反应所属的基本反应类型是( )
| A. | 分解反应 | B. | 化合反应 | C. | 置换反应 | D. | 复分解反应 |
 煤、石油和天然气是常见的三种化石燃料,它们属于不可再生能源.随着科学技术的发展以及生产和生活需求的增加,人们正在利用和开发其他新能源.
煤、石油和天然气是常见的三种化石燃料,它们属于不可再生能源.随着科学技术的发展以及生产和生活需求的增加,人们正在利用和开发其他新能源.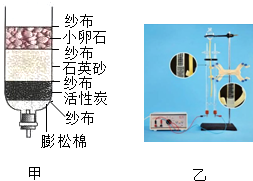 2016年3月22日是“世界水日”,水与人类的生活和生产密切相关.
2016年3月22日是“世界水日”,水与人类的生活和生产密切相关. 一包白色固体样品中可能含有Na2SO4、Na2CO3、NaCl中的一种或几种,为测定其成分,现进行如下实验:①取样品3.54g,加入适量水使其完全溶解;②先后逐滴加入BaCl2溶液、稀硝酸,产生沉淀的质量与时间的关系如图所示:
一包白色固体样品中可能含有Na2SO4、Na2CO3、NaCl中的一种或几种,为测定其成分,现进行如下实验:①取样品3.54g,加入适量水使其完全溶解;②先后逐滴加入BaCl2溶液、稀硝酸,产生沉淀的质量与时间的关系如图所示: