题目内容
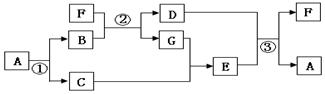
3.人类社会的发展需要充足的能源、丰富的材料、良好的环境.广阔的海洋中蕴含着无穷的资源,开发海洋,利用海洋成为人们关注的热点.利用粗盐,可以进一步获得纯碱.请你利用以下信息对相关问题进行研究.【生产流程】
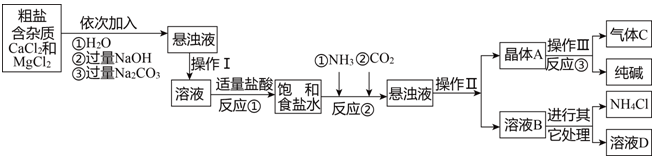
【产品与原理】
采用“侯氏制减法”生产工产品--纯碱和化肥NH4Cl.
生产原理是:将NH3和CO2通入饱和食盐水中得到NaHCO3和NH4Cl的混合物,反应为NaCl(饱和)+NH3+CO2+H2O=NaHCO3↓+NH4Cl;分离出NaHCO3,加热制得纯碱.
【相关资料】
已知20℃时有关物质的溶解度如下(气体值1体积水中能溶解的气体体积)
| 物质 | NaCl | NaHCO3 | NH4Cl | NH3 | CO2 |
| 溶解度 | 36.0g | 9.6g | 37.2g | 710g | 0.9g |
(1)操作Ⅰ、Ⅱ中,相同操作的名称为过滤.
(2)反应①中发生了2个反应.
(3)写出溶液B中除了NH4Cl的另一种溶质是碳酸氢钠.
(4)上述产生流程中可循环使用的是A(填序号).
A.挥发性气体CB.溶液BC.氢氧化镁D.化肥NH4Cl.
分析 (1)过滤能把固体和液体分离;
(2)稀盐酸和氢氧化钠反应生成氯化钠和水,和碳酸钠反应生成氯化钠、水和二氧化碳;
(3)析出碳酸氢钠的溶液仍然是碳酸氢钠的饱和溶液;
(4)碳酸氢钠受热分解生成碳酸钠、水和二氧化碳.
解答 解:(1)操作Ⅰ、Ⅱ中,相同操作的名称为过滤,通过过滤把液体和固体分离.
故填:过滤.
(2)反应①中,稀盐酸和氢氧化钠反应生成氯化钠和水,和碳酸钠反应生成氯化钠、水和二氧化碳,因此发生了2个反应.
故填:2.
(3)溶液B中除了NH4Cl的另一种溶质是碳酸氢钠,这是因为析出碳酸氢钠的溶液仍然是碳酸氢钠的饱和溶液.
故填:碳酸氢钠.
(4)上述产生流程中可循环使用的是碳酸氢钠受热分解生成的二氧化碳气体.
故填:A.
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论.

练习册系列答案
 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案
相关题目
19.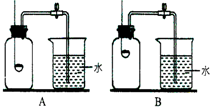 某校化学兴趣小组就空气中氧气的含量进行了如下实验探究
某校化学兴趣小组就空气中氧气的含量进行了如下实验探究
【集体讨论】(1)讨论后同学们认为,选择的药品既要能消耗氧气,又不会跟空气中的其他成分反应而且生成物为固体.他们应该选择B(填序号),为了充分消耗容器中的氧气,药品的用量应保证足量.
A、蜡烛 B、红磷 C、硫 D、木炭
(2)小组同学共同设计如图所示的两套装置,你认为合理的是A(填序号).为了确保实验的成功,在装药品之前应该检查装置的气密性.
【分组实验】在讨论的基础上,他们分组进行了实验.
【数据分析】实验结束后,整理数据如表:(注:集气瓶容积为100mL)
(3)通过对实验结果的交流,大多数同学都验证出氧气约占空气体积的$\frac{1}{5}$.通过实验还可以推断集气瓶中剩余气体的性质是不易溶于水、不能燃烧,不支持燃烧(写出两点)
 某校化学兴趣小组就空气中氧气的含量进行了如下实验探究
某校化学兴趣小组就空气中氧气的含量进行了如下实验探究【集体讨论】(1)讨论后同学们认为,选择的药品既要能消耗氧气,又不会跟空气中的其他成分反应而且生成物为固体.他们应该选择B(填序号),为了充分消耗容器中的氧气,药品的用量应保证足量.
A、蜡烛 B、红磷 C、硫 D、木炭
(2)小组同学共同设计如图所示的两套装置,你认为合理的是A(填序号).为了确保实验的成功,在装药品之前应该检查装置的气密性.
【分组实验】在讨论的基础上,他们分组进行了实验.
【数据分析】实验结束后,整理数据如表:(注:集气瓶容积为100mL)
| 组别 | 1 | 2 | 3 | 4 | 5 | 6 |
| 进入集气瓶中水的体积/mL | 20 | 21 | 19 | 20 | 22 | 19 |
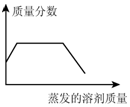
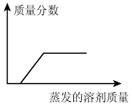
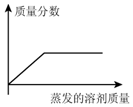
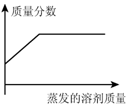
11.在温度保持t℃不变时,某物质M的溶液经过如下变化,下列结论正确的是( )
M溶液$→_{无晶体析出}^{蒸发20克水}$M1溶液$→_{析出5克晶体}^{再蒸发10克水}$M2溶液.
M溶液$→_{无晶体析出}^{蒸发20克水}$M1溶液$→_{析出5克晶体}^{再蒸发10克水}$M2溶液.
| A. | M溶液一定是不饱和溶液,M l溶液一定是饱和溶液 | |
| B. | Ml溶液、M2溶液都一定是饱和溶液 | |
| C. | t℃时M的溶液度一定是50克 | |
| D. | M1可能是饱和溶液,M2一定是饱和溶液 |
 雷电是一种常见的天气现象.2015年3月23日江西抚州市,雷声隆隆之后,数道闪 电划破夜空,场面十分壮观.
雷电是一种常见的天气现象.2015年3月23日江西抚州市,雷声隆隆之后,数道闪 电划破夜空,场面十分壮观.
 实验室常用MnO2与浓盐酸反应制备Cl2,其反应方程式为:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O反应装置如图甲(夹持装置已略去)
实验室常用MnO2与浓盐酸反应制备Cl2,其反应方程式为:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O反应装置如图甲(夹持装置已略去)