题目内容
16.CO与某气体M混合物含氧55%,则M可能是( )| A. | CO2 | B. | NO2 | C. | SO2 | D. | SO3 |
分析 由于CO中氧元素的质量分数为57%而混合气体中氧元素质量分数为55%,利用平均值法可判断混合物中另一种气体的氧元素质量分数小于55%.
解答 解:A、CO2中C、O元素质量比=12:(16×2)=3:8,而CO中C、O质量比为3:4,因此CO2中氧元素质量分数大于CO中氧元素质量分数,即大于57%;故A不正确;
B、NO2中O元素的质量分数=$\frac{16×2}{46}$×100%≈70%>55%,故B不正确;
C、SO2中S、O元素质量比=32:(16×2)=1:1,因此SO2中氧元素质量分数为50%,小于55%,故C正确;
D、SO3中S、O元素质量比=32:(16×3)=1:2,因此SO3中氧元素质量分数约为66.7%,大于55%,故D不正确;
故选:C.
点评 利用物质化学式组成上的特点,可以较为简单地判断其中元素质量分数的大小,使计算得以简化.

练习册系列答案
 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案
相关题目
6.下列关于碳及其化合物的说法正确的是( )
| A. | 焦炭还原氧化铜发生的是置换反应 | |
| B. | CO2的过量排放是导致酸雨的主要原因 | |
| C. | 铅笔字迹易变模糊是因为常温下石墨的化学性质活泼 | |
| D. | CO和CO2都是大气污染物 |
4.下列各组物质的溶液不用其它试剂就可鉴别的是( )
| A. | HCl、CuSO4、KNO3、Na2SO4 | B. | FeCl3、HCl、NaCl、NaOH | ||
| C. | CaCl2、K2CO3、HCl、(NH4)2CO3 | D. | NaNO3、Na2SO4、HCl、H2SO4 |
11.生活离不开科学,科学与我们生活息息相关,用下列生活中常见物质来完成下题要求:
A.甲烷 B.生石灰 C.熟石灰 D.乙醇 E硫酸铜晶体 F.蛋白质 G.硝酸铵
用物质的字母序号填空:属于盐的是EG.
A.甲烷 B.生石灰 C.熟石灰 D.乙醇 E硫酸铜晶体 F.蛋白质 G.硝酸铵
用物质的字母序号填空:属于盐的是EG.
1.浙江省提出“五水共治”策略,即治污水、防洪水、排涝水、保供水、抓节水,打造美丽江南水乡.下列措施与“五水共治”精神不符的是( )
| A. | 工业废水直接用于农业灌溉 | B. | 家庭中洗完的淘米水用于浇花 | ||
| C. | 水源地附近禁止禽畜养殖 | D. | 生活污水集中收集处理后排放 |
5.下列物质的说法中不正确的是( )
| A. | 用氢氧化钠溶液可以吸收二氧化碳气体 | |
| B. | 用氯化钡能区别稀盐酸和稀硫酸 | |
| C. | 用水可以区别浓硫酸和稀硫酸 | |
| D. | 用稀盐酸区别氢氧化钠溶液和石灰水 |
6.胆矾是一种蓝色晶体,受热时易失去结晶水,成为白色粉未;在工业上精炼铜、镀铜等过程中都需要胆矾.上述对胆矾的描述中.没有涉及到的是( )
| A. | 物理性质 | B. | 化学性质 | C. | 组成 | D. | 用途 |
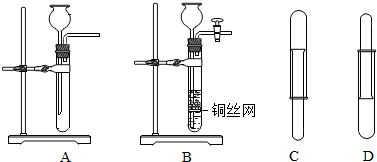
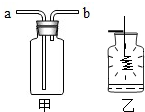 小科在实验室完成了氧气的制取并收集了一瓶氧气用来做铁丝在氧气中的燃烧实验.
小科在实验室完成了氧气的制取并收集了一瓶氧气用来做铁丝在氧气中的燃烧实验.