题目内容
1.将一定质量的铁和氧化铜的混合物粉末放入足量稀盐酸中,充分反应后产生气体0.4g,并得到残留固体6.4g.则原混合物粉末的质量是( )| A. | 8.0g | B. | 11.2g | C. | 16.0g | D. | 24.8g |
分析 将一定质量的铁和氧化铜的混合物粉末放入足量稀盐酸中,铁能与稀盐酸反应,氧化铜能与稀盐酸反应生成了氯化铜和水,铁能与氯化铜反应生成铜和氯化亚铁.根据生成氢气的质量求出与稀盐酸反应的铁的质量,根据生成铜的质量可求出与氯化铜反应的铁的质量,还可求出氧化铜的质量,将三者加在一起就是原混合物的质量.
解答 解:由题意可知,将一定质量的铁和氧化铜的混合物粉末放入足量稀盐酸中,铁能与稀盐酸反应生成氯化亚铁和氢气,氧化铜能与稀盐酸反应生成了氯化铜和水,铁能与氯化铜反应生成铜和氯化亚铁.
设与稀盐酸反应的铁的质量为x
Fe+2HCl═FeCl2+H2↑
56 2
x 0.4g
$\frac{56}{2}=\frac{x}{0.4g}$ 解得:x=11.2g
设与氯化铜反应的铁的质量为y
Fe+CuCl2═FeCl2+Cu
56 64
y 6.4g
$\frac{56}{64}=\frac{y}{6.4g}$ 解得:y=5.6g
氧化铜的质量为:6.4g÷($\frac{64}{80}×100%$)=8.0g
所以,原混合物的质量为:11.2g+5.6g+8.0g=24.8g
由以上计算分析可知,D正确.
故选D.
点评 本题主要考查了根据化学方程式的计算.解答本题的关键是分清铁和氧化铜的混合物粉末放入足量稀盐酸中,发生的反应有哪些,残留固体的成分是什么.

练习册系列答案
相关题目
3.咸宁城际铁路的建成将进一步推动我市经济的发展,在修建铁路的土石方爆破中要用到黑火药,黑火药爆炸时发生反应的化学方程式是2KNO3+3C+S$\frac{\underline{\;点燃\;}}{\;}$K2S+3CO2↑+X↑,根据以上信息,下列说法错误的是( )
| A. | X的化学式是N2 | B. | 黑火药在混合物 | ||
| C. | KNO3中氮元素的化合价为+5价 | D. | KNO3属于氨肥 |
4.下列课外实验中不涉及化学变化的是( )
| A. | 用点燃蜡烛的方法制炭黑 | |
| B. | 用食醋除水壶中水垢 | |
| C. | 用活性炭除冰箱中的异味 | |
| D. | 用柠檬酸、小苏打、白糖、凉开水自制汽水 |
1.小明同学患有夜盲症,到了晚上就看不清东西,引起夜盲症主要是人体内缺乏( )
| A. | 铁元素 | B. | 钙元素 | C. | 维生素A | D. | 维生素C |
8.根据下表中的数据,回答下列问题:
(1)20℃时KCl的溶解度是34.0g;
(2)20℃时将20g KCl与50g水混合,充分溶解后,所得溶液为饱和(填“饱和”或“不饱和”);
(3)上表两种物质中,KNO3的溶解度受温度的影响大.
| 温度/℃ | 20 | 40 | 60 | 80 | 100 | |
| 溶解度/g | KCl | 34.0 | 40.0 | 45.6 | 51.1 | 56.7 |
| KNO3 | 31.6 | 63.9 | 110 | 169 | 246 | |
(2)20℃时将20g KCl与50g水混合,充分溶解后,所得溶液为饱和(填“饱和”或“不饱和”);
(3)上表两种物质中,KNO3的溶解度受温度的影响大.
6.下列物质中常用作调味品的是( )
| A. | 氯化钠 | B. | 硫酸钠 | C. | 氢氧化钠 | D. | 硝酸钠 |
10.下列不能正确反映相关实验过程中量的变化关系的图象是( )
| A. | 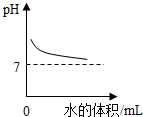 氢氧化钠溶液加水稀释 | |
| B. | 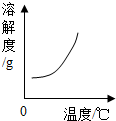 一定压强下,氧气在水中的溶解度 | |
| C. | 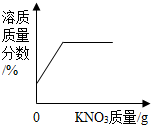 一定温度下,向不饱和硝酸钾溶液中加入硝酸钾 | |
| D. | 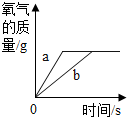 氯酸钾和二氧化锰混合加热制氧气中,a使用催化剂,b未使用催化剂 |
11.下列肥料属于复合肥料的是( )
| A. | NH4NO3 | B. | KNO3 | C. | KCl | D. | Ca(H2PO4)2 |