题目内容
在由CO和O2组成的混合气体中,测知碳元素的质量分数为18%,则混合气体中CO和O2的质量比为( )
A.2:1 B.1:2 C.29:21 D.21:29
【答案】
D
【解析】
试题分析:由题意知:CO和O2混合气体中含碳元素18%,而碳元素之来源于CO,故可先假设混合气体质量为单位1,CO的质量为X,则O2的质量为1-X。列式计算如下:
X·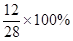 =1×18%
=1×18%
X=0.42
则:O2的质量为:1-0.42=0.58
所以:CO:O2=0.42:0.58=21:29
考点:有关化学式的计算和推断;化合物中某元素的质量计算。
点评:熟练掌握化学式中元素质量分数的计算,并理解混合物中碳元素只来自于CO,是解此题的关键。
【答案】C
【解析】乙是一种常见的气体化合物,能转化生成甲,则乙可能是二氧化碳,二氧化碳能转化生成碳酸盐,观察选项,故选C.

练习册系列答案
相关题目