题目内容
13. 水是人类生活中不可缺少的物质.
水是人类生活中不可缺少的物质.(1)下列净水方法中,通常用于除去水中难溶性杂质的是A
A.过滤B.煮沸C.蒸馏D.吸附
(2)为了探究水的组成,实验装置如图所示:
①该实验中,与两个电极相连的a、b两支玻璃管中产生的气体分别是H2和O2(填化学式),质量比为1:8.
②写出该反应的化学方程式2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑
(3)硬水给生活和生产带来很多麻烦,生活中常用肥皂水区分硬水和软水,常用煮沸方法降低水的硬度.
(4)水能灭火的原理是降低温度到可燃物的着火点以下.
分析 (1)根据过滤的原理分析判断;
(2)根据点哦及水实验的现象、结论及发生的反应分析回答;
(3)根据硬水和软水的区别及硬水的软化方法分析回答;
(4)根据灭火的原理分析回答.
解答 解:(1)在净水方法中,通常用于除去水中难溶性杂质的是过滤;
(2)①由电解水的实验装置图可知,与两个电极相连的a、b两支玻璃管中产生的气体分别是电源的负极、正极产生的气体,分别为H2 O2,质量比为1:8;
②电解水反应的化学方程式是:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑;
(3)硬水给生活和生产带来很多麻烦,生活中常用肥皂水区分硬水和软水,遇肥皂水水产生的泡沫少的是硬水,遇肥皂水水产生的泡沫多的是软水,常用煮沸方法降低水的硬度.
(4)由于水在蒸发时能吸收大量的热,所以水能灭火的原理是:降低温度到可燃物的着火点以下.
故答为:(1)A;(2)①H2,O2,1:8.②2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑;(3)肥皂水,煮沸.(4)降低温度到可燃物的着火点以下.
点评 本题主要考查了有关水的知识,属于课本中的基础知识,难度不大,根据已有的知识分析解答即可.

练习册系列答案
相关题目
8.对化学方程式4P+5O2 $\frac{\underline{\;点燃\;}}{\;}$2P2O5所表示的意义,下列说法正确的是( )
| A. | 4个磷跟5个氧气反应,生成两个五氧化二磷 | |
| B. | 磷加氧气等于五氧化二磷 | |
| C. | 磷元素与氧元素结合生成两个五氧化二磷 | |
| D. | 每4个磷原子可与5个氧分子反应生成两个五氧化二磷分子 |
18.用久置的镁条做实验时,需要用砂纸把表面的灰黑色打磨掉,直到露出光亮的银白色.实验小组同学对镁条表面“灰黑色外衣”的成分进行如下探究.
【提出问题】镁条表面“灰黑色外衣”的成分是什么?
【查阅资料】
Ⅰ.是镁与空气中的氧气反应生成的氧化镁.
Ⅱ.是镁与空气中的二氧化碳反应生成的黑色碳单质.
Ⅲ.根据铜锈的成分是碱式碳酸铜,推测镁条表面的“灰黑色外衣”是镁在潮湿的空气中生锈得到的碱式碳酸镁.
同学们经讨论,从颜色上否定了只含有氧化镁,因为氧化镁是白色的.
【查阅资料】
①碱式碳酸镁的性质有:受热可分解;常温下能与稀硫酸反应.
②白色的硫酸铜粉末遇水能变为蓝色.
③碳不与稀硫酸反应,但与浓硫酸在加热条件下能反应并生成CO2、SO2和H2O.同学们认为碳与浓硫酸反应生成三种产物的共同点是都属于氧化物(答出一点即可).
【进行实验】
(1)同学们用久置的镁粉进行了如下实验.
(2)同学们发现,经加热一段时间后,试管中镁粉会突然“噗”地燃烧起来,出现红热,很快停止,并有黑色固体粘附在试管壁上.
①将试管取下,冷却后加入足量稀硫酸,大部分固体溶解,并有气泡出现,但黑色固体没有消失.请写出有气体生成的一个反应化学方程式Mg+H2SO4═MgSO4+H2↑.
②将实验①试管中的混合物进行过滤_(填操作名称),除去其中溶液,向黑色固体中加入浓硫酸,加热.黑色固体全部溶解,得澄清溶液并伴有刺激性气味的气体产生.
实验(2)说明,镁在CO2中可以燃烧,生成了碳单质.
【实验结论】
综合上述实验现象,实验小组认为镁条表面“灰黑色外衣”中含有碳和碱式碳酸镁.
【反思与评价】
有的同学提出,实验(2)不足以证明镁条表面“灰黑色外衣”中含有碳,他的理由是久置的镁条是放置在常温下的空气环境中,实验(2)是将镁粉在加热且有二氧化碳生成的环境中.
【提出问题】镁条表面“灰黑色外衣”的成分是什么?
【查阅资料】
Ⅰ.是镁与空气中的氧气反应生成的氧化镁.
Ⅱ.是镁与空气中的二氧化碳反应生成的黑色碳单质.
Ⅲ.根据铜锈的成分是碱式碳酸铜,推测镁条表面的“灰黑色外衣”是镁在潮湿的空气中生锈得到的碱式碳酸镁.
同学们经讨论,从颜色上否定了只含有氧化镁,因为氧化镁是白色的.
【查阅资料】
①碱式碳酸镁的性质有:受热可分解;常温下能与稀硫酸反应.
②白色的硫酸铜粉末遇水能变为蓝色.
③碳不与稀硫酸反应,但与浓硫酸在加热条件下能反应并生成CO2、SO2和H2O.同学们认为碳与浓硫酸反应生成三种产物的共同点是都属于氧化物(答出一点即可).
【进行实验】
(1)同学们用久置的镁粉进行了如下实验.
实 验 装 置 | 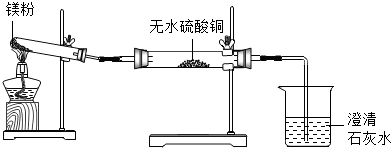 |
| 实 验 现 象 | ①无水硫酸铜粉末逐渐由白色变为蓝色 ②澄清石灰水变浑浊 |
结 论 | 久置的镁粉中除镁元素外,还含有的元素是C、H、O 久置的镁粉中含有碱式碳酸镁 |
①将试管取下,冷却后加入足量稀硫酸,大部分固体溶解,并有气泡出现,但黑色固体没有消失.请写出有气体生成的一个反应化学方程式Mg+H2SO4═MgSO4+H2↑.
②将实验①试管中的混合物进行过滤_(填操作名称),除去其中溶液,向黑色固体中加入浓硫酸,加热.黑色固体全部溶解,得澄清溶液并伴有刺激性气味的气体产生.
实验(2)说明,镁在CO2中可以燃烧,生成了碳单质.
【实验结论】
综合上述实验现象,实验小组认为镁条表面“灰黑色外衣”中含有碳和碱式碳酸镁.
【反思与评价】
有的同学提出,实验(2)不足以证明镁条表面“灰黑色外衣”中含有碳,他的理由是久置的镁条是放置在常温下的空气环境中,实验(2)是将镁粉在加热且有二氧化碳生成的环境中.


 阅读下面科普短文.
阅读下面科普短文.
 某实验小组设计了如图所示的实验装置,既可用于制取气体,又可用于探究物质性质.
某实验小组设计了如图所示的实验装置,既可用于制取气体,又可用于探究物质性质.