题目内容
下列现象及事实与相应的解释一致的是
| 现 象 及 事 实 | 解 释 | |
| A | 用水银温度计测量体温 | 温度升高,原子体积变大 |
| B | 浓硫酸溶于水放热 | 浓硫酸与水发生了化学反应 |
| C | 水通电分解与水受热沸腾有本质区别 | 化学变化中分子可分,物理变化分子不变 |
| D | 喝了汽水后,常常会打嗝 | 气体的溶解度随压强的减小而减小 |
C

 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案 A~F是初中化学常见的六种物质,它们之间的关系如下图所示。“ ”表示物质间的转化关系,“——”表示两种物质能相互反应(部分反应物、生成物及反应条件未标出)。A可以与酸、碱、盐三类物质发生反应,D是食盐的主要成分,C和F都是无色气体,反应①和②都有白色沉淀生成。
A~F是初中化学常见的六种物质,它们之间的关系如下图所示。“ ”表示物质间的转化关系,“——”表示两种物质能相互反应(部分反应物、生成物及反应条件未标出)。A可以与酸、碱、盐三类物质发生反应,D是食盐的主要成分,C和F都是无色气体,反应①和②都有白色沉淀生成。
 |
⑴F的化学式为  ;
;
⑵写出B→E反应的化学方程式 ;
⑶写出A与一种碱反应的化学方程式 。
合金在生活中应用十分广泛。已知某合金粉末除含铝外,还含有铁、铜中的一种或两种。小明利用下图装置对合金粉末中铁、铜的存在进行探究时,误把氢氧化钠溶液当成稀硫酸加入到锥形瓶中,他惊奇的发现有无色气体放出,注射器活塞向右移动。
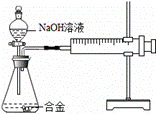
【提出疑问】
难道NaOH溶液也能与某些金属发生化学反应吗?
【查阅资料】
(1)铝能与氢氧化钠溶液反应,铁、铜不能与氢氧化钠溶液反应。
(2)铝与氢氧化钠溶液反应的化学方程式为:
2Al+2NaOH+2H2O═2NaAlO2+3H2↑(NaAlO2 溶于水,溶液显无色)
【进行猜想】
猜想1:该合金粉末除铝外,还含有铁。
猜想2:该合金粉末中除铝外,还含有 。
猜想3:该合金粉末中除铝外,还含有铁、铜。
【实验探究】
下列实验仅供选用的试剂:20%的硫酸溶液、30%的NaOH溶液。实验记录如下:
| 实验步骤 | 实验现象 | 实验结论 |
| ①取一定量的合金粉末,加过量的 ,充分反应后过滤,滤渣备用 | 粉末部分溶解,并有无色气体放出 | 合金中一定含有
|
| ②取步骤①所得滤渣,加过量的____,充分反应 | 滤渣部分溶解,并有无色气体放出,溶液呈浅绿色 | 合金中一定含有
|
【交流反思】
1.一般来说,活泼金属能与稀硫酸等酸反应,而铝与酸、碱都能反应,说明铝具有特殊的性质。铝与稀硫酸反应的化学方程式是__________________________。
2.若小明一开始向合金粉末中加入的是足量的稀硫酸,则最终剩余的固体成分是 。
【后续探究】
小明找到一块废旧的镁铝合金,积极探究其组成。他取32g铝镁合金样品,将120g氢氧化钠溶液平均分成三份依次加入样品中(2Al+2NaOH+2H2O═2NaAlO2+3H2↑,镁与氢氧化钠溶液不反应),充分反应后,过滤出固体,将其洗涤、干燥、称量,得实验数据如下:
| 所加氢氧化钠溶液的次数 | 第一次 | 第二次 | 第三次 |
| 剩余固体的质量/g | 21.2 | 10.4 | 8.0 |
计算:(1)该合金中,铝元素与镁元素的质量比是____________。
(2)所用氢氧化钠溶液中溶质的质量分数。(写出计算过程)




