题目内容
如图是碳还原氧化铜的实验装置,相关说法错误的是( )
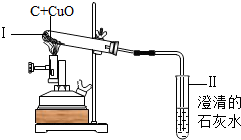

| A、反应前碳粉与氧化铜应充分混合 |
| B、Ⅱ中澄清石灰水变浑浊 |
| C、理论上Ⅰ中减少的质量可能等于Ⅱ中增加的质量 |
| D、反应结束时应先停止加热,待冷却后再将导管移出试管 |
考点:碳的化学性质
专题:碳单质与含碳化合物的性质与用途
分析:A.反应物接触充分,反应速率越快;
B.根据反应的产物来分析;
C.根据质量守恒定律来分析;
D.根据该实验中的注意事项来分析.
B.根据反应的产物来分析;
C.根据质量守恒定律来分析;
D.根据该实验中的注意事项来分析.
解答:解:A.在反应前,将碳粉与氧化铜充分混合,在化学反应时,速率越快,故正确;
B.实验中产生了二氧化碳,通入石灰水后,看到变浑浊,故正确;
C.根据质量守恒定律,Ⅰ中固体减少的质量就是生成二氧化碳的质量,而Ⅱ中增重的质量就是吸收二氧化碳的质量,因此相等,故正确;
D.实验结束后,要先将导管取出,在停止加热,以免冷水倒吸炸裂试管,故错误.
故选D.
B.实验中产生了二氧化碳,通入石灰水后,看到变浑浊,故正确;
C.根据质量守恒定律,Ⅰ中固体减少的质量就是生成二氧化碳的质量,而Ⅱ中增重的质量就是吸收二氧化碳的质量,因此相等,故正确;
D.实验结束后,要先将导管取出,在停止加热,以免冷水倒吸炸裂试管,故错误.
故选D.
点评:实验过程中需要注意的问题很多,要对各种实验有一个比较前面的理解,为设计实验、进行实验、分析实验奠定基础.

练习册系列答案
相关题目
生活中常见的物质里属于溶液的是( )
| A、蒸馏水 | B、石灰浆 |
| C、牛奶 | D、生理盐水 |
向一个密封容器中放入M、N、Q、P四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表,其中正确的是( )
| 物质 | M | N | Q | P |
| 反应前质量(g) | 18 | 1 | 2 | 32 |
| 反应后质量(g) | X | 26 | 2 | 12 |
| A、该反应的基本反应类型属于分解反应 |
| B、反应后物质M的物质的质量为13g |
| C、反应中M、P均为反应物 |
| D、物质Q一定是该反应的催化剂 |
硝酸钾的溶解度如下图所示,有关叙述正确的是( )
| 温度(℃) | 20 | 30 | 40 | 50 | 60 |
| 溶解度(g/100g水) | 31.6 | 45.8 | 63.9 | 85.5 | 110 |
| A、20℃时,可配成50g35%的硝酸钾饱和溶液 |
| B、30℃和50℃时,等质量的硝酸钾饱和溶液,所含水的体积,前者大于后者 |
| C、40℃时,50g硝酸钾饱和溶液降温至20℃,析出固体的质量为32.3g |
| D、60℃时,50g硝酸钾饱和溶液中,溶质与溶剂的质量比为11:21 |
物质对应的用途错误的是( )
| A、稀有气体:多用途电光源 |
| B、氧气:高能燃料 |
| C、二氧化碳:光合作用 |
| D、石灰石:生产生石灰 |
能够说明分子在不断运动的现象是( )
| A、蜡炬成灰 | B、花香四溢 |
| C、大雨倾盆 | D、木已成舟 |