题目内容
7.甲、乙、丙是三个实验的示意图,根据图中所示,回答下列问题.
(1)写出乙中反应的化学方程式:4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.
(2)计算甲中1.6g的硫完全燃烧生成二氧化硫的质量:3.2g.
(3)描述丙集气瓶中铁燃烧的现象:剧烈燃烧、火星四射、生成了黑色固体物质,放出了大量的热.
分析 (1)根据磷燃烧生成了五氧化二磷分析;
(2)根据硫燃烧的反应,由硫质量计算生成二氧化硫的质量;
(3)根据铁丝在氧气中燃烧的现象分析回答.
解答 解:(1)磷燃烧生成五氧化二磷,反应的化学方程式是:4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5;
(2)设生成的二氧化硫的质量为x
S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2
32 32
1.6g x
$\frac{16}{32}=\frac{1.6g}{x}$ 解得:x=3.2g
(3)丙集气瓶中铁燃烧的现象是:剧烈燃烧、火星四射、生成了黑色固体物质,放出了大量的热.
故答案为:(1)4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5;(2)3.2g;(3)剧烈燃烧、火星四射、生成了黑色固体物质,放
点评 解答本题的关键是了解常见物质在氧气中燃烧的反应、现象等方面的知识,熟练掌握化学方程式的书写及基本计算等知识.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
15.小红同学向盐酸与氯化钡的混合溶液中逐滴滴入碳酸钠溶液至过量,记录滴入的碳酸钠溶液的质量(x)与有关量的变化关系如图所示.下列判断正确的是( )
| A. | 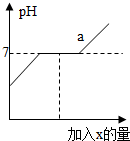  当碳酸钠溶液加至a点时,溶液中Na2CO3正与BaCl2发生反应 | |
| B. |  当碳酸钠溶液加至b点时,溶液中HCl与Na2CO3恰好反应完全 | |
| C. |  当碳酸钠溶液加至c点时,溶液中含有的溶质是氯化钠和氯化钡 | |
| D. |  当碳酸钠溶液加至d点时,溶液中BaCl2与Na2CO3恰好反应完全 |
13.区别一瓶蒸馏水和一瓶矿泉水,不能使用的方法是( )
| A. | 蒸发 | B. | 加肥皂水 | C. | 尝味道 | D. | 测导电性 |
2.下列解决问题的方法可行的是( )
| 要解决的问题 | 所用方法 | |
| A | 土壤呈酸性 | 撒适量的氢氧化钠改良酸性土壤 |
| B | 除去CO2中混有少量的CO | 点燃 |
| C | 干燥湿润的CO2气体 | 将气体通过氢氧化钠固体 |
| D | 鉴别羊毛织物与腈纶织物 | 燃烧后闻气味 |
| A. | A | B. | B | C. | C | D. | D |
16.我市某校初三(1)班学生去湖光岩春游,带回了几小块石灰石样品.为了检测样品中碳酸钙的含量,甲、乙、丙、丁四位同学用质量分数相同的盐酸与样品充分反应来讲行实验测定(样品中的杂质不溶于水,且不与盐酸反应).测得数据如表:
试回答:10g样品与足量稀盐酸反应后可产生二氧化碳多少克?
| 甲同学 | 乙同学 | 丙同学 | 丁同学 | |
| 所取石灰石样品质量(g) | 10 | 10 | 10 | 10 |
| 加入盐酸的质量(g) | 20 | 30 | 45 | 50 |
| 剩余固体的质量(g) | 6 | 4 | 1 | 1 |