题目内容
金属与盐溶液之间的反应,一般是活动性较强的金属可把活动性较弱的金属从其盐溶液中置换出来,如铜和硝酸银溶液反应,其化学方程式为 铝与硫酸铜溶液反应,化学方程式为 ,这两个反应都是 反应.
考点:金属的化学性质,反应类型的判定,书写化学方程式、文字表达式、电离方程式
专题:金属与金属材料
分析:根据在金属活动性顺序中,排在氢前面的金属,能够和稀盐酸、稀硫酸发生置换反应,生成氢气和相应的盐;排在金属活动性顺序前面的金属,能够把排在后面的金属从它的盐溶液中置换出来等知识进行分析.
解答:解:铜和硝酸银反应生成硝酸铜和银,化学方程式为:Cu+2AgNO3═2Ag+Cu(NO3)2,铝和硫酸铜反应生成硫酸铝和铜,化学方程式为:2Al+3CuSO4=Al2(SO4)3+3Cu,两个反应均满足置换反应的条件,属于置换反应.
故答案为:Cu+2AgNO3═2Ag+Cu(NO3)2,2Al+3CuSO4=Al2(SO4)3+3Cu,置换.
故答案为:Cu+2AgNO3═2Ag+Cu(NO3)2,2Al+3CuSO4=Al2(SO4)3+3Cu,置换.
点评:本题主要考查了金属活动性顺序的应用和化学方程式的书写,难度不大,在平时多加记忆即可.

练习册系列答案
 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案
相关题目
下列方法中能用于区别硬水和软水的( )
| A、观察颜色 | B、加入明矾 |
| C、加漂白粉 | D、加肥皂水 |
“钻石恒久远,一颗永流传”这句广告词体现的钻石的性质是( )
| A、密度大 | B、化学性质稳定 |
| C、熔点高 | D、外观美丽 |
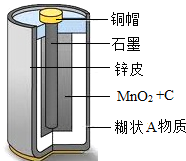 随意丢弃废旧干电池会造成环境污染,而废旧干电池中的许多物质都是可以回收利用的.请根据如图回答下列问题:
随意丢弃废旧干电池会造成环境污染,而废旧干电池中的许多物质都是可以回收利用的.请根据如图回答下列问题: