题目内容
10.将10g铜锌合金放入盛有150g稀硫酸溶液的烧杯中,恰好完全反应后,称得烧杯内的物质的总质量为159.8g.请计算:(1)生成氢气的质量是0.2 g.
(2)反应后溶液中溶质的质量分数.
分析 根据反应的化学方程式进行计算,铁和铜加入稀硫酸中只有锌和稀硫酸反应,总质量减少的量就是生成的氢气的质量.
解答 解:(1)反应后产生的氢气质量为:10g+150g-159.8g=0.2g;
(2)设恰好完全反应生成硫酸锌的质量为x,参加反应的锌的质量为y
Zn+H2SO4═ZnSO4+H2↑
65 161 2
y x 0.2 g
$\frac{161}{2}$=$\frac{x}{0.2g}$ x=16.1 g
$\frac{65}{2}$=$\frac{y}{0.2g}$ y=6.5 g
反应后溶液中溶质的质量分数为:
$\frac{16.1g}{159.8g-?10g-6.5g?}$×100%=10.3%
答案:
(1)0.2;
(2)反应后溶液中溶质的质量分数为10.3%.
点评 本题考查了根据化学方程式的计算,完成此题,可以依据反应的化学方程式进行.

练习册系列答案
 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案
相关题目
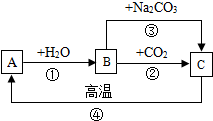 A、B、C是三种常见的含钙化合物.它们之间有如图所示的转化关系(部分产物略去).
A、B、C是三种常见的含钙化合物.它们之间有如图所示的转化关系(部分产物略去). 已知A、B、C、D、E均为初中化学常见物质,其中,E通常为气体,它们相互转化的关系如图所示.请结合下列情况回答有关问题:
已知A、B、C、D、E均为初中化学常见物质,其中,E通常为气体,它们相互转化的关系如图所示.请结合下列情况回答有关问题: 回答下列有关Zn、Fe、Cu、Ag的相关问题:
回答下列有关Zn、Fe、Cu、Ag的相关问题: