题目内容
请根据如图所示的实验过程和提供的数据(步骤②产生的气体全部逸出),回答下列问题: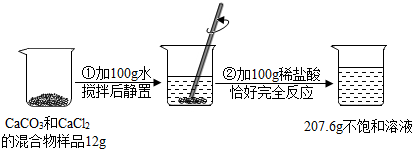
(1)产生二氧化碳 g.
(2)计算原混合物样品中CaCO3的质量分数(写出计算过程)

(1)产生二氧化碳
(2)计算原混合物样品中CaCO3的质量分数(写出计算过程)
考点:根据化学反应方程式的计算
专题:综合计算(图像型、表格型、情景型计算题)
分析:(1)根据图中信息可以知道,反应前加入的物质的总质量为:12g+100g+100g=212g,而反应后剩余物质的总质量为207.6g,根据质量守恒定律可以知道物质减少的质量为生成二氧化碳的质量;
(2)根据二氧化碳的质量结合化学方程式可以求算出碳酸钙的质量,据此解答碳酸钙的质量分数即可.
(2)根据二氧化碳的质量结合化学方程式可以求算出碳酸钙的质量,据此解答碳酸钙的质量分数即可.
解答:解:
(1)反应中生成CO2的质量为:12g+100g+100g-207.6g=4.4g;
(2)设原混合物中 CaCO3的质量为x
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x 4.4g
=
x=10g
原混合物样品中CaCO3的质量分数
×100%≈83.3%
答案:
(1)4.4
(2)原混合物样品中CaCO3的质量分数83.3%
(1)反应中生成CO2的质量为:12g+100g+100g-207.6g=4.4g;
(2)设原混合物中 CaCO3的质量为x
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x 4.4g
| 100 |
| 44 |
| x |
| 4.4g |
x=10g
原混合物样品中CaCO3的质量分数
| 10g |
| 12g |
答案:
(1)4.4
(2)原混合物样品中CaCO3的质量分数83.3%
点评:要想解答好这类题目,首先,要理解和熟记根据化学反应方程式的计算步骤和格式,以及与之相关的知识等.然后,根据所给的问题情景或图表信息等,结合所学的相关知识和技能,细致地分析题意(或图表信息)等各种信息资源,并细心地探究、推理后,按照题目要求进行认真地选择或解答即可

练习册系列答案
 期末集结号系列答案
期末集结号系列答案
相关题目
下列说法,正确的是( )
| A、1g食盐完全溶解在100g水中,得到溶质质量分数为1%食盐水溶液 |
| B、把1g面粉放入100g水里搅拌,得到101g 面粉水溶液 |
| C、10mL酒精与20mL水混合后,得到30mL酒精水溶液 |
| D、把1滴植物油滴入10mL汽油中充分振荡,可以得到溶液 |
用判断镁条在氧气中燃烧发生了化学变化的主要依据是( )
| A、剧烈燃烧 |
| B、耀眼的强光 |
| C、放出大量的热 |
| D、生成一种白色固体物质 |
一个密闭容器中加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,测得数据见下表.下列说法中正确的是( )
| 物质质量 | 甲 | 乙 | 丙 | 丁 |
| 反应前 | 25g | x | 5g | 5g |
| 反应后 | 8g | 23g | 5g | 8g |
| A、x=14 g |
| B、该反应是化合反应 |
| C、在该反应中,丙物质一定做催化剂 |
| D、若甲和丁的相对分子质量分别为34和18,则甲、丁的化学计量数比为3:1 |
 如图所示:
如图所示: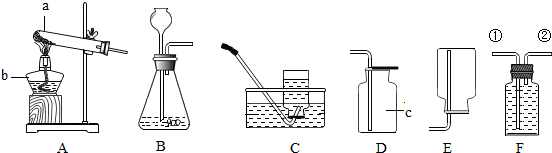
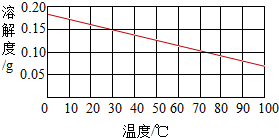 如图是熟石灰的溶解度曲线.
如图是熟石灰的溶解度曲线.