题目内容
15.碳酸钙粉末与稀盐酸混合后,产生气泡,一段时间后.固体粉末消失.(1)写出上述反应的化学方程式.
(2)假设得到的气体全部从溶液中排出,则反应后得到的溶液中,除水之外,还可能含有哪些物质?请你对该问题做出全面合理的猜想,并写出你的猜想:CaCl2和HCl
(3)设计实验验证你的猜想,并完成下列表格的填写
| 实验操作 | 预期的实验现象和结论 |
分析 (1)根据碳酸钙与稀盐酸反应的原理来分析;
(2)根据反应后的溶液中的溶质可能性来分析;
(3)根据酸性溶液的检验方法来分析.
解答 解:(1)碳酸钙与稀盐酸反应生成氯化钙、水和二氧化碳,故填:CaCO3+2HCl═CaCl2+H2O+CO2↑;
(2)因为碳酸钙粉末完全消失了,所以可能是恰好完全反应,也可能是盐酸过量;所以溶液中的溶质可能只有氯化钙,也可能是氯化钙和氯化氢;故填:CaCl2和HCl;
(3)氯化钙溶液显中性,盐酸显酸性,可用紫色的石蕊试液来检验,故填:
| 实验操作 | 预期的实验现象和结论 |
| 取少量反应后的溶液于试管中,滴加紫色的石蕊试液 | 若石蕊试液不变色,则溶液中的溶质只有CaCl2; 若石蕊试液变红色,则溶液中的溶质有CaCl2和HCl. |
点评 本题考查了常见物质的鉴别,在做此类题时,首先弄清所要鉴别的物质的不同性质,然后选择适当的试剂进行鉴别,出现不同的现象,在分析化学反应后所得物质的成分时,除考虑生成物外还需考虑反应物的过量问题.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
5.下列仪器中,能用酒精灯直接加热的有( )
①试管 ②集气瓶 ③蒸发皿 ④量筒 ⑤烧杯 ⑥燃烧匙 ⑦石棉网.
①试管 ②集气瓶 ③蒸发皿 ④量筒 ⑤烧杯 ⑥燃烧匙 ⑦石棉网.
| A. | ①③④⑥ | B. | ①②⑤⑦ | C. | ①③⑥⑦ | D. | ②③⑤⑥ |
9.某彩金是在黄金中加入铜、银等熔炼而成的合金,常用于制造首饰.从物质分类的角度看,彩金属于( )
| A. | 混合物 | B. | 纯净物 | C. | 单质 | D. | 化合物 |
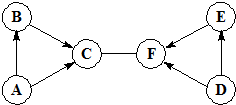 A、B、C、D、E、F是初中化学上册常见的六种物质,它们之间有如图所示的关系,箭头表示一种物质可以转化成另一种物质,C和F能反应.其中A、B、C含有一种相同的元素,D、E、F含有另一种相同的元素.
A、B、C、D、E、F是初中化学上册常见的六种物质,它们之间有如图所示的关系,箭头表示一种物质可以转化成另一种物质,C和F能反应.其中A、B、C含有一种相同的元素,D、E、F含有另一种相同的元素.