题目内容
20.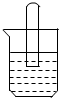 将一个充满二氧化碳的试管倒立在盛有紫色石蕊溶液的烧杯中,一段时间后可以观察到的现象是:(1)试管内上升一段液柱;紫色石蕊试液变红;
将一个充满二氧化碳的试管倒立在盛有紫色石蕊溶液的烧杯中,一段时间后可以观察到的现象是:(1)试管内上升一段液柱;紫色石蕊试液变红; (2)再用拇指堵住试管口,取出试管对该试管内的液体加热,则观察到有气泡冒出,写出该反应的化学方程式为:H2CO3$\frac{\underline{\;\;△\;\;}}{\;}$H2O+CO2↑.
分析 二氧化碳能与水反应生成碳酸,使试管内气体压强减小,再根据酸使石蕊试液变色情况进行分析,加热时碳酸很不稳定能分解,再考虑变色情况,根据方程式的书写方法写出方程式.
解答 解:二氧化碳能与水反应生成碳酸,使试管内气体压强减小,在外界大气压的作用下液体被压入试管内,所以试管内液面上升,碳酸属于酸,酸能使紫色石蕊试液变红;由于碳酸很不稳定,加热时碳酸分解生成水和二氧化碳,所以红色溶液又变成了原来的颜色紫色,反应物是碳酸,生成物是水和二氧化碳,二氧化碳后面标上上升符号,所以方程式是:H2CO3$\frac{\underline{\;\;△\;\;}}{\;}$H2O+CO2↑.
故答案为:
试管内上升一段液柱;紫色石蕊试液变红;H2CO3$\frac{\underline{\;\;△\;\;}}{\;}$H2O+CO2↑.
点评 解答本题关键是要知道二氧化碳与谁反应生成碳酸,酸能使紫色石蕊试液变红,碳酸不稳定,能分解生成水和二氧化碳.

练习册系列答案
 小学课时作业全通练案系列答案
小学课时作业全通练案系列答案 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
单元全能练考卷系列答案
相关题目
10.将一小块银白色的金属钠放置在空气中会发生下列变化:
钠(Na) $\stackrel{O_{2}}{→}$钠的氧化物$\stackrel{H_{2}O}{→}$ 氢氧化钠溶液 $\stackrel{CO_{2}}{→}$白色固体
【提出问题】:常温下钠与氧气反应,产物有哪些?
【查阅资料】:钠的氧化物,除氧化钠(Na2O)外还有过氧化钠(Na2O2),氧化钠与过氧化钠都能与水发生反应,方程式如下:
Na2O+H2O=2NaOH;2Na2O2+2H2O=4NaOH+O2↑
【作出猜想】:常温下钠与氧气反应的产物.
猜想1:Na2O,
猜想2:Na2O2,
猜想3:Na2O和Na2O2
【实验探究一】:
【继续探究】:钠在空气中放置一段时间得到白色固体的成分
【作出猜想】
猜想一:Na2CO3
猜想二:Na2CO3和NaOH
【实验探究二】:
【实验反思】
(1)过氧化钠也能与盐酸反应,方程式为:2Na2O2+4HCl=4NaCl+2H2O+X,X的化学式为O2.
(3)久置的固体氢氧化钠变质的原因是(用化学方程式表示)2NaOH+CO2═Na2CO3+H2O.
钠(Na) $\stackrel{O_{2}}{→}$钠的氧化物$\stackrel{H_{2}O}{→}$ 氢氧化钠溶液 $\stackrel{CO_{2}}{→}$白色固体
【提出问题】:常温下钠与氧气反应,产物有哪些?
【查阅资料】:钠的氧化物,除氧化钠(Na2O)外还有过氧化钠(Na2O2),氧化钠与过氧化钠都能与水发生反应,方程式如下:
Na2O+H2O=2NaOH;2Na2O2+2H2O=4NaOH+O2↑
【作出猜想】:常温下钠与氧气反应的产物.
猜想1:Na2O,
猜想2:Na2O2,
猜想3:Na2O和Na2O2
【实验探究一】:
| 实验操作 | 实验现象 | 实验结论 |
| 取少量钠的氧化物加入足量蒸馏水 | 没有气泡生成 | 猜想1正确 |
【作出猜想】
猜想一:Na2CO3
猜想二:Na2CO3和NaOH
【实验探究二】:
| 实验操作 | 实验现象 | 实验结论 |
| 1.取少量白色固体加入足量氯化钙溶液 | 产生白色沉淀 | 白色固体成分为Na2CO3和NaOH |
| 2.过滤、取少量滤液加入无色的酚酞试液 | 变成红色 |
(1)过氧化钠也能与盐酸反应,方程式为:2Na2O2+4HCl=4NaCl+2H2O+X,X的化学式为O2.
(3)久置的固体氢氧化钠变质的原因是(用化学方程式表示)2NaOH+CO2═Na2CO3+H2O.
11.所示图中取用药品正确的是( )
| A. |  | B. | 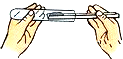 | C. | 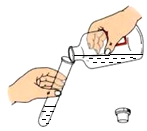 | D. |  |
5.下列物质的用途与其化学性质无关的是( )
| A. | 氧气供给呼吸 | B. | 用一氧化碳冶炼金属 | ||
| C. | 用活性炭做净水器的滤芯 | D. | 用二氧化碳灭火 |