题目内容
实验室用玻璃瓶存放氢氧化钠试剂时,常用 瓶塞.这是因为玻璃中含有一种叫二氧化硅的氧化物,二氧化硅的化学性质与二氧化碳相似,它可与氢氧化钠发生反应,化学方程式为 ,生成的产物溶液又叫玻璃胶,可以使瓶塞与玻璃牢牢地粘合在一起而难开启.
考点:碱的化学性质,书写化学方程式、文字表达式、电离方程式
专题:常见的碱 碱的通性
分析:根据题意,实验室盛放氢氧化钠溶液的试剂瓶不能用玻璃塞,因为氢氧化钠与玻璃中的二氧化硅缓慢地发生反应,两者反应生成硅酸钠和水,写出反应的化学方程式即可.
解答:解:实验室盛放氢氧化钠溶液的试剂瓶不能用玻璃塞,其原因是在常温下,氢氧化钠与玻璃中的二氧化硅缓慢地发生反应,两者反应生成硅酸钠和水,反应的化学方程式为:2NaOH+SiO2═Na2SiO3+H2O.
故答案为:
橡胶;2NaOH+SiO2═Na2SiO3+H2O.
故答案为:
橡胶;2NaOH+SiO2═Na2SiO3+H2O.
点评:本题难度不大,考查学生根据反应原理书写化学方程式的能力,化学方程式书写经常出现的错误有不符合客观事实、不遵守质量守恒定律、不写条件、不标符号等.

练习册系列答案
 初中暑期衔接系列答案
初中暑期衔接系列答案
相关题目
下列各组固体物质,只用水和组内物质就可相互鉴别的一组是( )
| A、FeCl3,Na2SO4,NaOH,AgNO3 |
| B、CaCO3,Na2CO3,K2CO3,BaCl2 |
| C、NaOH,KNO3,CuSO4,NaNO3 |
| D、BaCl2,CuSO4,MgCl2,NaCl |
A、B、C三种物质各15g,它们化合时只生成新物质D30g.若再增加10g A,最后反应物中只剩余C.据上述条件推断下列说法中正确的是( )
| A、第一次反应停止,B余下9克 |
| B、第二次反应后,C余下5克 |
| C、反应中A和C的质量比为5:3 |
| D、反应中B和C的质量比为3:1 |
在物质混合、反应等过程中,存在着“1+1≠2”的有趣现象.通常情况下,下列各种混合或反应过程中,“1+1=2”的是( )
| A、1g硫与1g氧气反应后生成物的质量 |
| B、1g酒精与1g水混合后的总质量 |
| C、1g硫酸钠溶液与1g氯化钡溶液混合后溶液的总质量 |
| D、1g饱和氯化钠溶液中加入1g氯化钠后所得溶液的质量 |
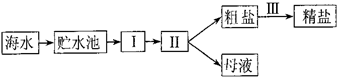
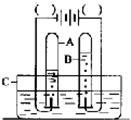 如图是电解水的示意图.
如图是电解水的示意图.