题目内容
11.为了测定石灰石样品中碳酸钙的质量分数,某兴趣小组的同学称取石灰石样品52g,放于烧杯中,逐渐滴加稀盐酸,使之与样品充分反应,恰好完全反应时(杂质不参加反应),加入稀盐酸的质量为180g,反应后烧杯中物质的总质量为210g.请计算:(1)生成二氧化碳的质量是22g;
(2)石灰石样品中碳酸钙的质量分数(结果保留到0.1%).
分析 分析所发生的反应,可发现反应后总质量减轻是由于生成了气体二氧化碳,根据质量守恒定律可求出二氧化碳的质量.然后利用二氧化碳的质量,根据反应的化学方程式,计算恰好完全反应时碳酸钙的质量,最后使用质量分数的计算公式,求出样品中碳酸钙的质量分数.
解答 解:生成二氧化碳的质量=52g+180g-210g=22g;
设样品中CaCO3的质量为x,
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x 22g
$\frac{100}{x}=\frac{44}{22g}$
x=50g
石灰石样品中碳酸钙的质量分数=$\frac{50g}{52g}×$100%≈96.1%
答案:
(1)22;
(2)石灰石样品中碳酸钙的质量分数为96.1%.
点评 根据反应的化学方程式能表示反应中各物质的质量关系,由反应中某物质的质量可计算出反应中其它物质的质量.

练习册系列答案
 百年学典课时学练测系列答案
百年学典课时学练测系列答案
相关题目
2.某兴趣小组为探究Ag、Fe、Cu三种金属的活动性顺序,设计下列实验,可以达到实验目的组合是( )
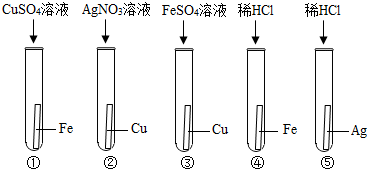

| A. | ①② | B. | ②④ | C. | ④⑤ | D. | ②③ |
19.下列相应物质的pH中,酸性最强的是( )
| A. | 液体肥皂(9.5-10.5) | B. | 酱油(4.0-5.0) | ||
| C. | 鸡蛋清(7.6-8.0) | D. | 柠檬汁(2.0-3.0) |
20.金属钠在空气中燃烧,可以生成淡黄色固体过氧化钠(Na2O2),Na2O2中氧元素的化合价为( )
| A. | -1 | B. | -2 | C. | +1 | D. | +2 |
1.下列有关物质燃烧现象的叙述中,正确的是( )
| A. | 铁丝在氧气中燃烧:火星四射,生成红色固体 | |
| B. | 硫粉在空气中燃烧:产生淡蓝色火焰,生成一种刺激性气味的气体 | |
| C. | 镁条在氧气中燃烧:发出耀眼的白光,生成白色的氧化镁固体 | |
| D. | 红磷在空气中燃烧:发出白光,生成大量的白色烟雾 |