题目内容
18.水是人类最宝贵的资源.按要求回答下列问题:(1)水是由水分子直接构成的.
(2)检验地下水是硬水还是软水,可用的物质是肥皂水.
(3)生活中既能降低水的硬度又能杀菌的方法是煮沸.
(4)能证明“水是由氢元素和氧元素组成”的实验是电解水实验.
(5)海水中含量最多的金属元素的名称是钠
(6)写出水具有的化学性质通电可分解.
分析 (1)根据水的构成进行分析;
(2)根据日常生活中用肥皂水来区分硬水与软水进行分析;
(3)根据生活中既能降低水的硬度又能杀菌的方法是煮沸进行分析;
(4)根据水通电分解生成氢气和氧气,所以该实验能证明水是由氢元素和氧元素组成
进行分析;
(5)根据海水中含量最多的金属元素进行分析;
(6)根据化学性质需要发生化学变化表现出来进行分析.
解答 解:(1)水是水分子由直接构成的;
(2)检验地下水是硬水还是软水,可用的物质是肥皂水;
(3)生活中既能降低水的硬度又能杀菌的方法是煮沸;
(4)水的电解生成了氢气和氧气,说明了水是由氢元素和氧元素组成的;
(5)海水中含量最多的金属元素是钠元素;
(6)在通电的条件下能分解生成氢气和氧气,需要发生化学变化表现,属于水的化学性质;
故答案为:(1)水分子;(2)肥皂水;(3)煮沸;(4)电解水实验;(5)钠;(6)通电可分解.
点评 本题考查了水的有关知识,完成此题,可以依据已有的知识进行解答.

练习册系列答案
相关题目
8. 向一定量的碳酸钾溶液中缓慢滴加稀盐酸,并不断搅拌.随着盐酸的加入,溶液中离子数目也相应地发生变化.如图所示,四条曲线与溶液中的离子的对应关系,完全正确的( )
向一定量的碳酸钾溶液中缓慢滴加稀盐酸,并不断搅拌.随着盐酸的加入,溶液中离子数目也相应地发生变化.如图所示,四条曲线与溶液中的离子的对应关系,完全正确的( )
 向一定量的碳酸钾溶液中缓慢滴加稀盐酸,并不断搅拌.随着盐酸的加入,溶液中离子数目也相应地发生变化.如图所示,四条曲线与溶液中的离子的对应关系,完全正确的( )
向一定量的碳酸钾溶液中缓慢滴加稀盐酸,并不断搅拌.随着盐酸的加入,溶液中离子数目也相应地发生变化.如图所示,四条曲线与溶液中的离子的对应关系,完全正确的( )| a | b | c | d | |
| A | Cl- | K+ | CO32- | HCO3- |
| B | K+ | CO32- | HCO3- | Cl- |
| C | K+ | CO32- | Cl- | HCO3- |
| D | K+ | HCO3- | Cl- | CO32- |
| A. | A | B. | B | C. | C | D. | D |
2.(1)将甲、乙、丙、丁四种物质放入密闭容器中,充分反应.各物质的化学式及质量变化如下表:
若甲、乙、丙、丁的相对分子质量之比为14:16:22:9,则该反应的化学方程式可表示为A+3B=2C+2D.
(2)M物质由Cu元素和O元素组成,其相对分子质量为144,且Cu、O元素的质量比为8:1,则M物质的化学式为Cu2O.
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 化学式 | A | B | C | D |
| 反应前质量(g) | 28 | 102 | 4 | 4 |
| 反应后质量(g) | 0 | 6 | 92 | 未知 |
(2)M物质由Cu元素和O元素组成,其相对分子质量为144,且Cu、O元素的质量比为8:1,则M物质的化学式为Cu2O.
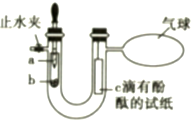 某同学在学完《分子和原子》后,对教材中的实验进行了如图所示的改进:
某同学在学完《分子和原子》后,对教材中的实验进行了如图所示的改进: