题目内容
5.(1)燃气安全是家庭生活中的头等大事.为了防止燃气泄漏,常在燃气中加入少量有特殊气味的乙硫醇(C2H5SH).乙硫醇充分燃烧时生成二氧化碳、二氧化硫和水,乙硫醇燃烧的化学方程式为2C2H5SH+9O2$\frac{\underline{\;点燃\;}}{\;}$2SO2+4CO2+6H20.(2)变色眼镜的玻璃片中含溴化银(AgBr),溴化银见光分解为银和单质溴(Br2),眼镜片自动变暗.光线弱时,单质溴与银又化合生成溴化银,眼镜片变亮.试写出避光时的化学方程式2Ag+Br2═2AgBr.
(3)新型材料的研制与应用推动了现代高新技术的发展.氮化硅(Si3N4)是一种高温陶瓷材料,工业上制氮化硅的方法是:用单质硅(Si)和氮气在高温条件下反应生成氮化硅,写出该反应的化学方程式3Si+2N2$\frac{\underline{\;高温\;}}{\;}$Si3N4.
分析 首先根据题意找出反应物和生成物以及反应条件,然后根据书写化学方程式的方法来分析解答;
解答 解:(1)乙硫醇充分燃烧即乙硫醇与氧气在点燃的条件下发生反应,产生二氧化碳、二氧化硫和水,化学方程式为2C2H5SH+9O2$\frac{\underline{\;点燃\;}}{\;}$2SO2+4CO2+6H20(2)光线弱时,单质溴与银又化合生成溴化银,反应的化学方程式为:2Ag+Br2═2AgBr.
(3)由题意,反应物为硅和氮气,生成物为氮化硅,反应条件为高温,故反应的化学方程式为:3Si+2N2$\frac{\underline{\;高温\;}}{\;}$Si3N4;
故答案为:(1)2C2H5SH+9O2$\frac{\underline{\;点燃\;}}{\;}$2SO2+4CO2+6H20;(2)2Ag+Br2═2AgBr;(3)3Si+2N2$\frac{\underline{\;高温\;}}{\;}$Si3N4;
点评 本题难度不大,考查学生根据反应原理书写化学方程式的能力,化学方程式书写经常出现的错误有不符合客观事实、不遵守质量守恒定律、不写条件、不标符号等.

练习册系列答案
 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
相关题目
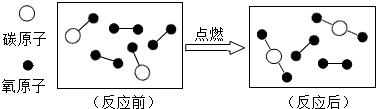
20.如图为某反应的微观示意图,则下列说法不正确的是( )

| A. | 反应后的物质是混合物 | |
| B. | 参加反应的CO、O2、CO2的分子个数比为2:3:2 | |
| C. | 该反应属于化合反应 | |
| D. | 反应前后原子的种类、数目都没有发生改变 |
17.等离子空气净化器在工作时会产生臭氧(O3),臭氧是一种公认的高效空气杀菌剂,但达到一定浓度时对人体也有害,不仅有臭味,也可能致癌.下列说法正确的是( )
| A. | 臭氧转变为氧气是物理变化 | |
| B. | 臭氧能吸收紫外线,保护地球上的生物免受紫外线的伤害 | |
| C. | 臭氧能杀菌,所以空气中臭氧浓度越高越好 | |
| D. | 等质量的臭氧和氧气含有相同分子数 |
15.以下各类盐中,除钾盐、钠盐、铵盐能溶于水外,其余大部分不溶于水的盐是
①盐酸盐 ②硫酸盐 ③硝酸盐 ④碳酸盐 ⑤磷酸盐( )
①盐酸盐 ②硫酸盐 ③硝酸盐 ④碳酸盐 ⑤磷酸盐( )
| A. | ①⑤ | B. | ②④ | C. | ③④ | D. | ④⑤ |

 在某公共场所,有如图广告:
在某公共场所,有如图广告: 某化肥包装袋上的部分说明如图所示.
某化肥包装袋上的部分说明如图所示.