题目内容
元素周期表示学习化学的重要工具.下表是元素周期表的一部分,请按表中信息回答问题:
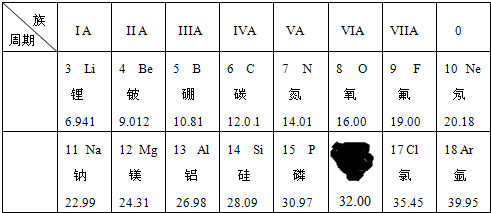
(1)图中有一种元素信息展示不完整,该元素位于元素周期表第 周期,属于 元素(填“金属”或“非金属”)、
(2)图Ⅰ是地壳中的元素含量(质量分数),图中C元素的名称是 ,D元素的符号是 .

(3)图Ⅱ是镓(Ga)的原子结构示意图,则镓的核电荷数x为 ,根据原子结构示意图判断,Ga与氯元素结合形成化合物,其化合物的化学式与下列物质可能相似的是 ;
A.NaCl B.CaCl2 C.AlCl3
(4)具有相同原子数和电子总数的分子或离子叫等电子体,等电子体具有相似的结构和性质,由上表中的数据判断下列各组粒子中属于等电子体的是
A.NO和O2 B.CO和OH- C.SO2和CO2 D.CO32-和NO3-
(5)在一个化学反应中,如果有元素化合价升高,同时就有元素化合价降低.探究钠元素的单质与水反应的生成物.甲同学猜想生成物为NaOH和H2;乙同学猜想生成物为NaOH和O2,从化合价的角度分析,你认为 同学的猜想是合理的.

(1)图中有一种元素信息展示不完整,该元素位于元素周期表第
(2)图Ⅰ是地壳中的元素含量(质量分数),图中C元素的名称是

(3)图Ⅱ是镓(Ga)的原子结构示意图,则镓的核电荷数x为
A.NaCl B.CaCl2 C.AlCl3
(4)具有相同原子数和电子总数的分子或离子叫等电子体,等电子体具有相似的结构和性质,由上表中的数据判断下列各组粒子中属于等电子体的是
A.NO和O2 B.CO和OH- C.SO2和CO2 D.CO32-和NO3-
(5)在一个化学反应中,如果有元素化合价升高,同时就有元素化合价降低.探究钠元素的单质与水反应的生成物.甲同学猜想生成物为NaOH和H2;乙同学猜想生成物为NaOH和O2,从化合价的角度分析,你认为
考点:元素周期表的特点及其应用,原子结构示意图与离子结构示意图,地壳中元素的分布与含量
专题:化学用语和质量守恒定律
分析:(1)根据元素周期律:电子层数等于周期数;族数值与该原子的最外层电子数相同;进行解答.
(2)根据化学元素汉字名称的偏旁可辨别元素的种类和题中的图表进行分析解答本题;
(3)元素的化学性质与最外层电子数有关,所以最外层电子数相同的元素化学性质相似;镓(Ga)元素与B元素最外层电子数相同,所以镓(Ga)元素与B元素的化学性质相似
(4)可以根据等电子体的特点方面进行分析、判断,从而得出正确的结论.磷酸根和硫酸根的原子个数和电子个数都相等,属于等电子体.NO和O2的原子数相同,但是电子数不相同.SO2和CO2的原子数相同,但是电子数不相同.
(5)根据题意可知“化学反应中,如果有元素化合价升高,同时就有元素化合价降低”,结合这句话从化合价的升高和降低来分析即可.
(2)根据化学元素汉字名称的偏旁可辨别元素的种类和题中的图表进行分析解答本题;
(3)元素的化学性质与最外层电子数有关,所以最外层电子数相同的元素化学性质相似;镓(Ga)元素与B元素最外层电子数相同,所以镓(Ga)元素与B元素的化学性质相似
(4)可以根据等电子体的特点方面进行分析、判断,从而得出正确的结论.磷酸根和硫酸根的原子个数和电子个数都相等,属于等电子体.NO和O2的原子数相同,但是电子数不相同.SO2和CO2的原子数相同,但是电子数不相同.
(5)根据题意可知“化学反应中,如果有元素化合价升高,同时就有元素化合价降低”,结合这句话从化合价的升高和降低来分析即可.
解答:解:(1)根据元素周期律:电子层数等于周期数;族数值与该原子的最外层电子数相同;可知这种元素位于元素周期表的第三周期,为硫元素,故为非金属元素;
(2)根据图中表示的地壳里所含各种元素的质量分数可知,图中C元素的名称是铝,D元素的符号是Fe.
(3)元素的化学性质与最外层电子数有关,所以最外层电子数相同的元素化学性质相似;镓(Ga)元素与Al元素最外层电子数相同,所以形成的氧化物与氧化铝的性质相似,故填:①
(4)A、一氧化氮和氧气的电子数分别是15和16,不属于等电子体.
B、一氧化碳和OH- 的电子个数不相等,不属于等电子体.
C、二氧化硫和二氧化碳的电子数分别是32和22,不属于等电子体.
D、CO32-和NO3- 的原子个数和电子个数都相等,属于等电子体.
故选D.
(5)甲同学的猜想合理.原因:若生成NaOH和O2,则该反应中钠元素的化合价由0价升高到十l价,氧元素的化合价由-2价升高到0价,只有元素化合价升高,没有元素化合价降低;
故答案为:
(1)三;非金属,(2)铝,Fe.(3)31,C;(4)D,(5)甲
(2)根据图中表示的地壳里所含各种元素的质量分数可知,图中C元素的名称是铝,D元素的符号是Fe.
(3)元素的化学性质与最外层电子数有关,所以最外层电子数相同的元素化学性质相似;镓(Ga)元素与Al元素最外层电子数相同,所以形成的氧化物与氧化铝的性质相似,故填:①
(4)A、一氧化氮和氧气的电子数分别是15和16,不属于等电子体.
B、一氧化碳和OH- 的电子个数不相等,不属于等电子体.
C、二氧化硫和二氧化碳的电子数分别是32和22,不属于等电子体.
D、CO32-和NO3- 的原子个数和电子个数都相等,属于等电子体.
故选D.
(5)甲同学的猜想合理.原因:若生成NaOH和O2,则该反应中钠元素的化合价由0价升高到十l价,氧元素的化合价由-2价升高到0价,只有元素化合价升高,没有元素化合价降低;
故答案为:
(1)三;非金属,(2)铝,Fe.(3)31,C;(4)D,(5)甲
点评:解答本题的关键是要充分理解等电子体的本质特征,只有这样才能对问题做出正确的判断.

练习册系列答案
 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案
相关题目
下列有关溶液的计算说法不正确的是( )
| A、在某温度下,将35g KCl溶液蒸干得到7gKCl固体,则原溶液溶质质量分数为20% |
| B、把100g 98%浓硫酸稀释至10%稀硫酸,外加水的质量为880g |
| C、把50g10% NaCl溶液变为20%的NaCl溶液,需蒸发掉25g水 |
| D、在20℃时将40g KNO3充分溶解在100g水中,仍然有8.4g KNO3不溶.所得溶液中KNO3质量分数是31.6% |
下列说法不正确的是( )
| A、实验室里常用稀盐酸与大理石反应来制取少量二氧化碳气体 |
| B、“电解水实验”表明水是由氢元素和氧元素组成的 |
| C、铁丝在空气中剧烈燃烧,火星四射,生成黄色固体,放出大量的热 |
| D、资料介绍,成年人缺钙易得软骨病,这里的“钙”是指钙元素 |
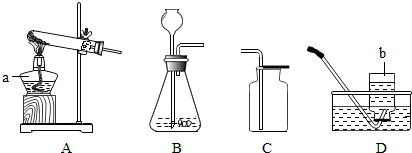
正确的化学实验操作对实验结果、人身安全非常重要.如图中的实验操作正确的是( )
A、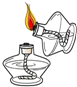 点燃酒精灯 |
B、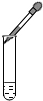 滴加液体 |
C、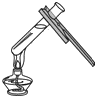 加热液体 |
D、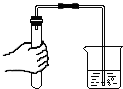 检查气密性 |
下列实验操作中能达到预期目的是( )
| A、用10mL水和20mL纯酒精混合配制成30mL酒精溶液 |
| B、将碳酸钙、活性炭、水混合后,常温下发生化合反应生成纯净的二氧化碳 |
| C、用托盘天平称取5.62g食盐 |
| D、用10mL量筒量取7.5mL稀盐酸 |
下列关于分子和原子的说法不正确的是( )
| A、分子在不停地运动 |
| B、分子在化学反应前后种类和数目保持不变 |
| C、原子可以直接构成物质 |
| D、原子是化学变化中的最小粒子 |
水是生命的基础,没有水就没有生命,下列有关水的说法正确的是( )
| A、水由两个氢元素和一个氧元素组成 |
| B、无色,无臭,清澈透明的水就是纯水 |
| C、通电分解水生成的氧气和氢气的体积比为1:2 |
| D、可以大量开采地下水以满足社会对水的需求 |
下列化学符号既能代表一种元素,又能代表一个原子,还能代表一种单质的是( )
| A、Cl | B、O | C、2H | D、Fe |