题目内容
9.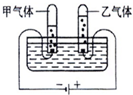 如图是水的电解实验装置图.
如图是水的电解实验装置图.(1)甲气体是氢气.
(2)写出电解水的方程式2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑.
(3)判断生活用水是硬水还是软水,可加入肥皂水进行检验.
(4)高铁酸钠(Na2FeO4)是一种新型高效净水剂,高铁酸钠中铁元素化合价为+6.
分析 (1)根据电解水时正阳负氢分析回答;
(2)根据电解水的反应分析回答;
(3)根据硬水和软水的鉴别方法分析回答;
(4)根据化合价原则求出元素的化合价.
解答 解:(1)由水的电解实验装置图可知,甲气体是电源的负极产生的是氢气.
(2)电解水生成了氢气和氧气,反应的方程式是:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑.
(3)判断生活用水是硬水还是软水,可加入肥皂水进行检验,遇肥皂水产生的泡沫少的是硬水,遇肥皂水产生的泡沫多的是软水.
(4)在高铁酸钠(Na2FeO4)中,钠元素显+1价,氧元素显-2价,设铁元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+1)×2+x+(-2)×4=0,则x=+6价.
故答为:(1)氢气;(2)2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑;(3)肥皂水;(4)+6.
点评 本题较为简单,了解电解水的现象合金结论、硬水与软水的鉴别、化合价原则即可分析解答.

练习册系列答案
相关题目
17.如图是甲、乙、丙三种固体物质的溶解度曲线,下列说法不正确的是( )
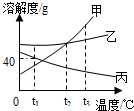

| A. | t2℃时,甲、乙两种物质的溶解度相等 | |
| B. | 甲的溶解度随温度的升高而增大 | |
| C. | 将t3℃时的丙的饱和溶液降温至t2℃时溶液变为不饱和溶液 | |
| D. | t1℃时,丙的饱和溶液中溶质的质量分数为40% |
4.如图是某化学反应的微观示意图,不同的圆球代表不同原子,下列说法中正确的是( )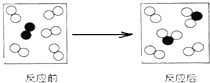

| A. | 该反应属于分解反应 | |
| B. | 参加反应的两种分子的个数比为5:1 | |
| C. | 该反应前后所有元素的化合价都没有变化 | |
| D. | 不考虑反应条件,该图示可表示氢气燃烧的反应 |
 某生产化肥碳酸氢铵(NH4HCO3)的企业,做了一个大型户外广告:
某生产化肥碳酸氢铵(NH4HCO3)的企业,做了一个大型户外广告: