题目内容
7.纳米碳酸钡是一种重要的无机化工产品,如图是生产纳米碳酸钡的工艺流程,请回答下列问题: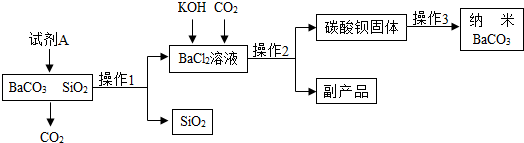
(1)试剂A名称是稀盐酸,试写出其与BaCO3反应的化学方程式BaCO3+2HCl═BaCl2+H2O+CO2↑.
(2)操作1名称为过滤,操作2所得主要副产物为KCl(填化学式),操作3为洗涤、检验和烘干,其中洗涤的作用是除去碳酸钡固体表面的杂质,检验洗涤是否干净可选用试剂为AgNO3(填化学式)溶液.
(3)上述流程中可循环利用的物质是CO2.
(4)资料:二氧化硅难溶于水,但可以和氢氧化钠、氢氟酸等物质反应.某同学根据资料重新设计方案提纯碳酸钡:取碳酸钡和二氧化硅混合物,滴加足量的氢氧化钠溶液,过滤,洗涤,烘干得碳酸钡固体.
分析 (1)根据碳酸钡能与稀盐酸反应生成氯化钡、水、二氧化碳分析;
(2)根据过滤可用于分离难溶性的物质,氢氧化钾和二氧化碳生成碳酸钾和水,碳酸钾和氯化钡反应生成碳酸钡白色沉淀和氯化钾,氯化钾与硝酸银可产生白色氯化银沉淀,可采取滴加硝酸银的方法检验洗涤干净;
(3)根据可循环利用的物质的特点:既是某反应的生成物又是另外反应的反应物,利用流程图判断其中循环利用的物质;
(4)利用二氧化硅与碳酸钡分析.
解答 解:(1)根据反应后生成氯化钡,由碳酸钡能与盐酸反应生成氯化钡、水、二氧化碳,可判断所加入的试剂A应为稀盐酸,反应的化学方程式为BaCO3+2HCl═BaCl2+H2O+CO2↑;
(2)根据操作后得到溶液与固体,利用过滤操作的特点,可判断操作1为过滤;氢氧化钾和二氧化碳生成碳酸钾和水,碳酸钾和氯化钡反应生成碳酸钡白色沉淀和氯化钾,所以操作2所得主要副产物为氯化钾;操作3为洗涤、检验和烘干,其中洗涤的作用是除去碳酸钡固体表面的杂质;操作为检验洗涤干净,利用氯化钾能与硝酸银产生白色沉淀,可向洗涤后的溶液中滴加硝酸银检验洗涤后的溶液中不再含有氯化钾,以证明洗涤干净;
(3)在向碳酸钡中加入稀盐酸时产生的二氧化碳气体可通入氯化钡溶液中,与氢氧化钾、氯化钡的混合溶液发生反应得到碳酸钡,即二氧化碳在过程中可进行循环利用;
(4)由题干可知“二氧化硅难溶于水,但可以和氢氧化钠、氢氟酸等物质反应”,又因为碳酸钡可以与氢氟酸反应,所以为除去碳酸钡与二氧化硅中的二氧化硅,利用二氧化硅能与氢氧化钠溶液反应生成可溶性的硅酸钠,可向混合物中加入过量氢氧化钠溶液以完全除去二氧化硅,经过过滤,洗涤,烘干得碳酸钡固体.
故答案为:
(1)稀盐酸;BaCO3+2HCl═BaCl2+H2O+CO2↑;
(2)过滤;KCl;除去碳酸钡固体表面的杂质;AgNO3;
(3)CO2;
(4)氢氧化钠溶液.
点评 通过流程图的分析,明确生产过程中所涉及的物质性质及变化规律,体现运用知识分析问题、解决问题的能力.

| A. | 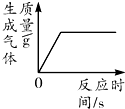 加热一定质量的高锰酸钾制取氧气 | |
| B. | 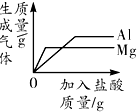 向等质量的铝粉和镁粉中分别滴入质量分数相同的足量的稀盐酸 | |
| C. | 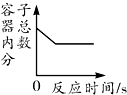 氢气和过量的氧气在密闭容器中完全反应 | |
| D. |  向一定质量的氯化铁和稀盐酸的混合溶液中逐滴滴加氢氧化钠溶液 |
| A. | 为提高农作物产量,大量使用化肥和农药 | |
| B. | 可利用氮气和氧气的沸点不同,分离液态空气制氧气 | |
| C. | “真金不怕火炼”是说黄金熔点很高 | |
| D. | 白色污染就是废弃的白色物质引起的污染 |
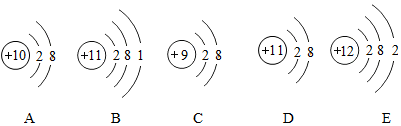
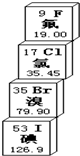 如图是从元素周期表第Ⅶ主族截取的局部图,图中的四种元素影响着我们的生活.下面是根据图示信息的一些说法,其中错误的是( )
如图是从元素周期表第Ⅶ主族截取的局部图,图中的四种元素影响着我们的生活.下面是根据图示信息的一些说法,其中错误的是( )| A. | 这四种元素都属于非金属元素 | B. | 这四种元素具有相似的化学性质 | ||
| C. | 1个氯原子的质量约是35.45g | D. | 氟原子核外电子数为9 |
| 选项 | 物质 | 少量杂质 | 除杂质的方法 |
| A | K2CO3溶液 | KCl | 加适量稀盐酸 |
| B | CaCl2溶液 | HCl | 加过量碳酸钙,过滤 |
| C | KCl固体 | MnO2 | 加水溶解,过滤 |
| D | CO2 | CO | 点燃 |
| A. | A | B. | B | C. | C | D. | D |