题目内容
15.向40g10%的氢氧化钠溶液中加入一定质量的硫酸铜溶液,恰好完全反应,所得物质的总质量为75.9g,请计算:(1)产生沉淀的质量;
(2)反应后所得溶液中溶质的质量分数.
分析 根据氢氧化钠与硫酸铜反应的方程式,由氢氧化钠的质量可求出生成的沉淀氢氧化铜的质量和硫酸钠的质量,在根据溶液的溶质质量分数计算即可.
解答 解:设:设生成的氢氧化铜的质量为x,硫酸钠的质量为y,
NaOH的质量为40g×10%═4g
2NaOH+CuSO4═Cu(OH)2↓+Na2SO4
80 98 142
4g X Y
$\frac{80}{4g}=\frac{98}{x}=\frac{142}{y}$
X═4.9g
Y═7.1g
所得溶液的质量为:75.9 g--4.9 g═71 g
反应后所得溶液中溶质的质量分数为:$\frac{7.1g}{71g}×100%$=10%.
答:反应后所得溶液中溶质的质量分数10%.
点评 本题考查根据化学方程式的计算及溶质质量分数的计算,解题是要注意,题中给出是所得混合物总质量,不是溶液的质量.溶液的质量应再减去沉淀的质量.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
5.下列装置所示的实验中,能达到实验目的是 ( )
| A. | 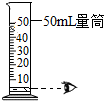 量取9.3mL稀盐酸 | B. | 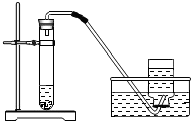 用石灰石与稀盐酸制取二氧化碳 | ||
| C. | 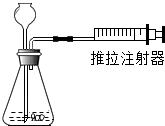 检查装置气密性 | D. | 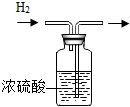 除去H2中的水蒸汽 |
4.“远离毒品,珍爱生命”!可卡因就是一种少量能使人昏睡,大量会使人死亡的毒品,其化学式为C17H31NO4.下列有关可卡因的叙述正确的是( )
| A. | 可卡因中氮氧元素的个数比为1:4 | |
| B. | 每个可卡因分子中含有43个原子核 | |
| C. | 可卡因是由碳、氢、氧原子构成的有机化合物 | |
| D. | 可卡因分子中含有17个碳原子、21个氢原子、1个氮原子和2个氧分子 |