题目内容
6.实验室有一瓶久置的固体,标签上写着“氢氧化钠”.为了检验里面是否还存在NaOH,实验员取少量该固体样品进行如图实验: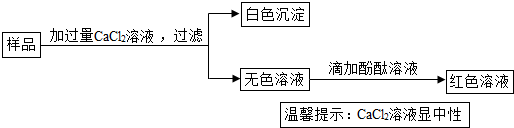
(1)根据溶液变红这一现象说明样品中含有C(填序号).
A.CaCl2 B.Na2CO3 C.NaOH D.Na2CO3和NaOH
(2)白色沉淀是CaCO3(填化学式).
分析 氢氧化钠能和空气中的二氧化碳反应生成碳酸钙沉淀和水,碳酸钠能和氯化钙反应生成碳酸钙沉淀和氯化钠,氢氧化钠溶液显碱性,能使酚酞试液变红色.
解答 解:加入过量氯化钙溶液后,碳酸钠完全反应,根据溶液变红这一现象说明样品中含有NaOH.
故填:C.
(2)白色沉淀是碳酸钠和氯化钙反应生成的CaCO3.
故填:CaCO3.
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
1.鉴别NaOH溶液,水和稀硫酸最简便的方法是( )
| A. | 加入Na2CO3溶液 | B. | 加入BaCl2溶液 | ||
| C. | 加入紫色石蕊试液 | D. | 加入无色酚酞试液 |
11.用一只大的玻璃缸,装上水,在缸里放几株水生植物,并用沙子固定,用漏斗把植物罩住.在一支试管里注满水,把试管慢慢倒过来罩在漏斗上,注意不要让空气进入试管.给予人工光照,在不断改变灯与植物的距离下进行测定.记录植物放出的气泡数目,结果如下:
在灯光的照射下,植物放出的气体是氧气.检验该气体的方法是用带火星的木条检验,能使带火星的木条复燃.
| 灯与植物之间的距离(厘米) | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
| 气泡个数(个/分钟) | 16 | 13 | 8 | 6 | 5 | 4 | 3 | 2 | 1 | 0 |
18.下列现象或操作与分子对应的特性不一致的选项是( )
| 选项 | 现象或操作 | 分子特性 |
| A | 水通直流电产生氢气和氧气 | 分子可以再分 |
| B | 10ml酒精与10ml水混合后总体积小于20ml | 分子间有间隔 |
| C | 桌子上的水滴一会儿没有了 | 分子在不断运动 |
| D | 充满气的车胎不易压缩 | 分子有一定的质量 |
| A. | A | B. | B | C. | C | D. | D |
15.下列对一些事实的解释不正确的是( )
| 事实 | 解释 | |
| A | 花香四溢 | 分子不断运动 |
| B | H2O2能杀菌消 毒而H2O则不能 | 两种物质的分子构成不同 |
| C | 温度计中的水银(汞)热胀冷缩 | 原子的大小发生改变 |
| D | 水和酒精混合后总体积变少 | 分子之间有空隙 |
| A. | A | B. | B | C. | C | D. | D |
 某兴趣小组利用如图所示装置测定石灰石样品中碳酸钙的质量分数,探究过程如下(注:石灰石样品中的杂质不参与反应也不溶解);
某兴趣小组利用如图所示装置测定石灰石样品中碳酸钙的质量分数,探究过程如下(注:石灰石样品中的杂质不参与反应也不溶解);