题目内容
在t℃时,将49g溶质的质量分数为l0%的H2SO4溶液与50g NaOH溶液混合,恰好完全反应,将反应后的溶液蒸发掉75g水,又恢复到t℃,溶液刚好达到饱和.试求:
(1)原NaOH溶液中溶质的质量分数;
(2)t℃时生成物的溶解度;
(3)所得饱和溶液的溶质质量分数.
(1)原NaOH溶液中溶质的质量分数;
(2)t℃时生成物的溶解度;
(3)所得饱和溶液的溶质质量分数.
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:溶质质量分数与化学方程式相结合的计算
分析:(1)根据硫酸的质量结合反应的化学方程式可以计算出氢氧化钠的质量,然后求出氢氧化钠溶液的质量分数即可;
(2)反应后得到的物质为硫酸钠,根据反应的化学方程式可以计算出其质量,然后结合溶解度的概念可以计算出气溶解度;
(3)根据溶液中溶质的质量分数的计算公式可以计算出所得溶液的溶质的质量分数.
(2)反应后得到的物质为硫酸钠,根据反应的化学方程式可以计算出其质量,然后结合溶解度的概念可以计算出气溶解度;
(3)根据溶液中溶质的质量分数的计算公式可以计算出所得溶液的溶质的质量分数.
解答:解:(1)49g溶质的质量分数为l0%的H2SO4溶液中硫酸的质量为:49g×10%=4.9g
设原NaOH溶液中溶质的质量为x,生成硫酸钠的质量为y
2NaOH+H2SO4═Na2SO4+2H2O
80 98 142
x 4.9g y
=
=
解得:x=4g y=7.1g
所以原NaOH溶液中溶质的质量分数为
×100%=8%;
(2)设t℃时生成物的溶解度为S
=
解得:S=42g;
(3)所得饱和溶液的溶质质量分数为:
×100%=29.6%.
答:(1)原NaOH溶液中溶质的质量分数为8%;
(2)t℃时生成物的溶解度为42g;
(3)所得饱和溶液的溶质质量分数为29.6%.
设原NaOH溶液中溶质的质量为x,生成硫酸钠的质量为y
2NaOH+H2SO4═Na2SO4+2H2O
80 98 142
x 4.9g y
| 80 |
| x |
| 142 |
| y |
| 98 |
| 4.9g |
解得:x=4g y=7.1g
所以原NaOH溶液中溶质的质量分数为
| 4g |
| 50g |
(2)设t℃时生成物的溶解度为S
| 7.1g |
| 49g+50g-75g |
| S |
| 100+S |
解得:S=42g;
(3)所得饱和溶液的溶质质量分数为:
| 7.1g |
| 49g+50g-75g |
答:(1)原NaOH溶液中溶质的质量分数为8%;
(2)t℃时生成物的溶解度为42g;
(3)所得饱和溶液的溶质质量分数为29.6%.
点评:此题是有关化学方程式及溶液的有关计算,涉及到已知反应物求生成物,溶液溶质质量分数的计算,解决此题对培养学生分析问题的能力有较好的帮助.

练习册系列答案
相关题目
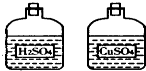 某同学用化学方法除掉一包铜、铁混合物中的铁,在实验台上有两瓶溶液(如图),从其中一瓶中取出100g溶液倒入烧杯中,他将该包混合物投入装有该溶液的烧杯中,恰好完全反应后过滤,得滤渣8.8克和溶液110.8克,求混合物中铁的质量分数.
某同学用化学方法除掉一包铜、铁混合物中的铁,在实验台上有两瓶溶液(如图),从其中一瓶中取出100g溶液倒入烧杯中,他将该包混合物投入装有该溶液的烧杯中,恰好完全反应后过滤,得滤渣8.8克和溶液110.8克,求混合物中铁的质量分数.