题目内容
18.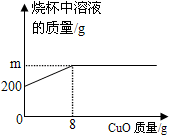 已知烧杯中装有200g硫酸和硫酸铜混合溶液,其中含硫酸铜4.8g.向烧杯中逐渐加入氧化铜,烧杯中溶液的质量与加入氧化铜的质量关系如图所示.当恰好完全反应时,所得的溶液为不饱和溶液.
已知烧杯中装有200g硫酸和硫酸铜混合溶液,其中含硫酸铜4.8g.向烧杯中逐渐加入氧化铜,烧杯中溶液的质量与加入氧化铜的质量关系如图所示.当恰好完全反应时,所得的溶液为不饱和溶液.(提示:CuO+H2SO4=CuSO4+H2O)请计算:
(1)m=208g.
(2)原混合溶液中H2SO4的质量分数.
(3)若取恰好完全反应时所得溶液10g配制成20%的硫酸铜溶液,需要30%的硫酸铜溶液多少克?
分析 (1)由图示可知氧化铜为8g,根据方程式可知氧化铜质量全部进入溶液;
(2)根据氧化铜的质量和方程式计算硫酸的质量,进一步计算原混合溶液中H2SO4的质量分数;
(3)根据溶液稀释或浓缩前后溶质的质量不变分析.
解答 解:(1)根据方程式CuO+H2SO4=CuSO4+H2O可知氧化铜质量全部进入溶液,所以m=200g+8g=208g;
(2)设混合溶液中H2SO4的质量为x,生成硫酸铜的质量为y
CuO+H2SO4=CuSO4+H2O
80 98 160
8g x y
$\frac{80}{8g}$=$\frac{98}{x}$=$\frac{160}{y}$
x=9.8g y=16g
原混合溶液中H2SO4的质量分数$\frac{9.8g}{200g}$×100%=4.9%;
(3)恰好完全反应时所得溶液溶质质量分数为$\frac{4.8g+16g}{208g}$×100%=10%
设需要30%的硫酸铜溶液z
10g×10%+z×30%=(10g+z)×20%
z=10g.
答:(1)208g;
(2)原混合溶液中H2SO4的质量分数4.9%;
(3)需要30%的硫酸铜溶液10g.
点评 本题是借助于数学模型,利用图表的方式来分析和解决化学计算中的有关问题,要求学生有较强的识图能力和数据分析能力.

练习册系列答案
 赢在课堂名师课时计划系列答案
赢在课堂名师课时计划系列答案
相关题目
8. 向一定量的硫酸铜溶液中加入一定质量分数的氢氧化钡溶液,直至过量.生成沉淀的质量与加入氢氧化钡溶液的质量关系如图所示,下列说法中正确的是( )
向一定量的硫酸铜溶液中加入一定质量分数的氢氧化钡溶液,直至过量.生成沉淀的质量与加入氢氧化钡溶液的质量关系如图所示,下列说法中正确的是( )
 向一定量的硫酸铜溶液中加入一定质量分数的氢氧化钡溶液,直至过量.生成沉淀的质量与加入氢氧化钡溶液的质量关系如图所示,下列说法中正确的是( )
向一定量的硫酸铜溶液中加入一定质量分数的氢氧化钡溶液,直至过量.生成沉淀的质量与加入氢氧化钡溶液的质量关系如图所示,下列说法中正确的是( )| A. | 0-a段只生成氢氧化铜沉淀 | |
| B. | 室温下,b点溶液的pH>7 | |
| C. | c点溶液中溶质至少有两种 | |
| D. | 整个过程中,溶液中氢元素的质量一直在增加 |
6.比较推理是化学学习中常用的思维方法,下列推理正确的是( )
| A. | 石墨能导电,故金刚石也能导电 | B. | 生铁比纯铁硬,故黄铜也比纯铜硬 | ||
| C. | 烧碱属于碱,故纯碱也属于碱 | D. | 碘难溶于水,故碘也难溶于汽油 |
3.进行下列对比实验,不需要控制变量的是( )
| A. | 用酚酞溶液鉴别稀硫酸和氢氧化钠溶液 | |
| B. | 用红磷和白磷探究可燃物燃烧的条件 | |
| C. | 用MnO2、CuO和H2O2溶液比较MnO2、CuO的催化效果 | |
| D. | 用镁、锌和稀盐酸比较镁、锌的金属活动性强弱 |
 用所学知识回答.
用所学知识回答.