题目内容
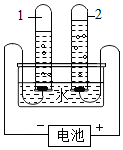
12.小红同学电解水实验时,观察到V(H2)=2:1,查资料得知:氢气的密度是0.0899g/L,氧气的密度是1.429g/L,她运用已学过的化学知识计算水的化学式.(1)电解水前向水中加入少量稀硫酸或氢氧化钠的目的是增强水的导电性.
(2)请你与她一起完成该计算,求出水的化学式(写出计算过程).
分析 (1)根据纯水的导电性较弱来分析;
(2)根据“正氧负氢,氢二氧一”,根据m=ρv,即可计算两者的质量比.根据化合物中元素的质量比=原子的相对原子质量×原子个数解答.
解答 解:(1)纯水的导电性较差,为了增强水的导电性,常向水中加入少量稀硫酸或氢氧化钠;故填:增强水的导电性;
(2)根据生成的氢气与氧气的体积比是2:1,根据m=ρv,可知氢气和氧气的质量比是$\frac{0.0899g/L×2}{1.429g/L×1}≈\frac{1}{8}$;水是由氢氧元素组成的,水中氢氧元素质量比为$\frac{1}{8}$.设水分子中氢原子的个数为x,氧原子的个数为y,则$\frac{1×x}{16×y}=\frac{1}{8}$,$\frac{x}{y}=\frac{2}{1}$,则水的化学式为H2O.
点评 要熟记正氧负氢,氢二氧一,依据有关的数据来计算水中氢氧元素的质量比,并推断水的化学式.

练习册系列答案
 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案 启东小题作业本系列答案
启东小题作业本系列答案
相关题目
3.某化学兴趣小组用火柴、蜡烛、烧杯三种实验材料探究物质燃烧的条件.
[提出问题]物质燃烧需要什么条件?
[猜想与假设]1.有可燃物 2.温度要达到着火点 3.与氧气(或空气)接触
[设计与实验]
[得出结论]猜想正确,燃烧必须同时满足三个条件,只要破坏一个燃烧的条件,就能达到灭火的目的.
[反思质疑]氢气在氯气中能燃烧.燃烧是否一定要有氧气参加?
[查阅资料1]镁条能在空气中剧烈燃烧,也能在二氧化碳中剧烈燃烧,发出耀眼的白光、放出大量的热;细铁丝可以在氯气中剧烈燃烧,放出大量的热,产生大量棕黄色的烟;磷能在氯气中剧烈燃烧,放出大量的热,产生大量的白色烟雾.
[表达与交流]
下列说法错误的是C(选填字母序号).
A.不是所有可燃物的燃烧都能用二氧化碳灭火
B.燃烧不一定要有氧气参加
C.镁条可以在二氧化碳中燃烧是因为二氧化碳分子中含的氧分子可助燃
D.镁条着火了不能用二氧化碳灭火
[反思质疑2]根据“细铁丝在氧气中燃烧”的实验现象,细铁丝在氧气中燃烧为什么会“火星四射”?
[查阅资料2]含碳细铁丝燃烧时,其中的炭粒生成的CO2气体在熔融液态物质中形成气泡,熔融液态物质因气泡炸裂引起“火星四射”的现象.
[设计实验]为了验证细铁丝在纯氧中燃烧产生“火星四射”现象的原因,你设计的实验方案是取长短相等,粗细相同的含碳细铁丝和不含碳的细铁丝,分别在氧气中燃烧,观察现象.
[提出问题]物质燃烧需要什么条件?
[猜想与假设]1.有可燃物 2.温度要达到着火点 3.与氧气(或空气)接触
[设计与实验]
| 验证 | 对比实验 | |
| 假设1 | 示例:加热烧杯,烧杯不可燃 | (仿例填写): |
| 假设2 | 常温放置蜡烛,蜡烛不能燃烧 | (仿例填写): |
| 假设3 | 点燃蜡烛,蜡烛在空气中持续燃烧 | (仿例填写): |
[反思质疑]氢气在氯气中能燃烧.燃烧是否一定要有氧气参加?
[查阅资料1]镁条能在空气中剧烈燃烧,也能在二氧化碳中剧烈燃烧,发出耀眼的白光、放出大量的热;细铁丝可以在氯气中剧烈燃烧,放出大量的热,产生大量棕黄色的烟;磷能在氯气中剧烈燃烧,放出大量的热,产生大量的白色烟雾.
[表达与交流]
下列说法错误的是C(选填字母序号).
A.不是所有可燃物的燃烧都能用二氧化碳灭火
B.燃烧不一定要有氧气参加
C.镁条可以在二氧化碳中燃烧是因为二氧化碳分子中含的氧分子可助燃
D.镁条着火了不能用二氧化碳灭火
[反思质疑2]根据“细铁丝在氧气中燃烧”的实验现象,细铁丝在氧气中燃烧为什么会“火星四射”?
[查阅资料2]含碳细铁丝燃烧时,其中的炭粒生成的CO2气体在熔融液态物质中形成气泡,熔融液态物质因气泡炸裂引起“火星四射”的现象.
[设计实验]为了验证细铁丝在纯氧中燃烧产生“火星四射”现象的原因,你设计的实验方案是取长短相等,粗细相同的含碳细铁丝和不含碳的细铁丝,分别在氧气中燃烧,观察现象.
7.下列关于水的说法不正确的是( )
| A. | 用活性炭可以除去水中的色素和异味 | |
| B. | 长期饮用蒸馏水不利于人体键康 | |
| C. | 明矾可促进浑水中悬浮杂质的沉降 | |
| D. | 过滤能除去天然水中所有的杂质 |
17.下列有关空气的说法错误的是( )
| A. | 按质量计算,空气中含有氮气约78%,氧气约21% | |
| B. | 空气是一种重要的自然资源 | |
| C. | 空气中分离出来的氮气,可作食品的防腐剂 | |
| D. | 空气中的稀有气体,化学性质非常稳定 |
1.下列用途利用了物质的物理性质的是( )
| A. | 铜丝做导线 | B. | 氢气可以做燃料 | ||
| C. | 氧气用于助燃剂 | D. | 二氧化碳可以做灭火器 |
 (1)根据物质初步分类的知识,在①双氧水的溶液;②液态氧;③四氧化三铁;④氯酸钾;⑤二氧化碳;⑥自来水;⑦铜粉中属于混合物的是①⑥(填序号,下同);属于纯净物的是②③④⑤⑦.属于单质的是②⑦;属于化合物的是③④⑤;属于氧化物的是③⑤.
(1)根据物质初步分类的知识,在①双氧水的溶液;②液态氧;③四氧化三铁;④氯酸钾;⑤二氧化碳;⑥自来水;⑦铜粉中属于混合物的是①⑥(填序号,下同);属于纯净物的是②③④⑤⑦.属于单质的是②⑦;属于化合物的是③④⑤;属于氧化物的是③⑤.