题目内容
小宇和小曼在用如图所示实验装置完成实验的过程中发现如下问题,请回答下列相关问题.

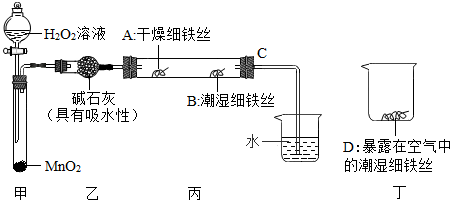
小宇设计的实验装置和选用药品如图A所示,小曼的如图B所示,他们在反应前后都进行了规范的操作,准确的称量和细致的观察.通过实验,小宇认为:在化学反应中,生成物的总质量与反应物的总质量不相等,小曼认为:在化学反应中,生成物的总质量与反应物的总质量相等,
①你认为结论正确的是 ,请你谈谈导致另一种结论错误的原因: .
②请完成图B的反应方程式
③图A的实验原理常用于实验室制取二氧化碳气体,但该装置目前显然不适宜用来制取二氧化碳气体,你认为要组成一套合理的装置,还需要用到的玻璃仪器有:导管(带双孔塞)、锥形瓶、玻璃片、 (此为一分).

小宇设计的实验装置和选用药品如图A所示,小曼的如图B所示,他们在反应前后都进行了规范的操作,准确的称量和细致的观察.通过实验,小宇认为:在化学反应中,生成物的总质量与反应物的总质量不相等,小曼认为:在化学反应中,生成物的总质量与反应物的总质量相等,
①你认为结论正确的是
②请完成图B的反应方程式
③图A的实验原理常用于实验室制取二氧化碳气体,但该装置目前显然不适宜用来制取二氧化碳气体,你认为要组成一套合理的装置,还需要用到的玻璃仪器有:导管(带双孔塞)、锥形瓶、玻璃片、
考点:质量守恒定律及其应用,书写化学方程式、文字表达式、电离方程式
专题:化学用语和质量守恒定律
分析:①根据盐酸和碳酸钙反应生成了氯化钙、水、二氧化碳,因为装置不密闭,所以有气体跑出质量减少,物质的总质量减小,所以不能用来验证质量守恒;稀盐酸溶液与氢氧化钠溶液反应生成氯化钠和水,没有物质跑出,质量不变,能验证质量守恒进行解答.
②正确书写稀盐酸与氢氧化钠的化学方程式.
③根据正确二氧化碳的装置和反应原理,选择实验仪器.
②正确书写稀盐酸与氢氧化钠的化学方程式.
③根据正确二氧化碳的装置和反应原理,选择实验仪器.
解答:解:
①由于小宇在操作过程中,碳酸钙与稀盐酸反应生成的CO2气体逸出烧杯,所以剩余的生成物的质量比反应物的总质量减少了,不能用来验证质量守恒定律;
小曼用的是稀盐酸溶液与氢氧化钠溶液反应生成氯化钠和水,没有气体跑出,所以反应前后物质的总质量相等.
②图B为稀盐酸与氢氧化钠溶液的反应,其反应方程式为:HCl+NaOH=NaCl+H2O.
③图A的实验原理常用于实验室制取二氧化碳气体,因为常温可以发生反应,故还需要用到的玻璃仪器有:导管(带双孔塞)、锥形瓶、玻璃片、长颈漏斗、集气瓶.
故答案为:
①小曼,碳酸钙与稀盐酸反应生成的CO2气体逸出烧杯,所以剩余的生成物的质量比反应物的总质量减少了.
②HCl+NaOH=NaCl+H2O
③长颈漏斗、集气瓶.
①由于小宇在操作过程中,碳酸钙与稀盐酸反应生成的CO2气体逸出烧杯,所以剩余的生成物的质量比反应物的总质量减少了,不能用来验证质量守恒定律;
小曼用的是稀盐酸溶液与氢氧化钠溶液反应生成氯化钠和水,没有气体跑出,所以反应前后物质的总质量相等.
②图B为稀盐酸与氢氧化钠溶液的反应,其反应方程式为:HCl+NaOH=NaCl+H2O.
③图A的实验原理常用于实验室制取二氧化碳气体,因为常温可以发生反应,故还需要用到的玻璃仪器有:导管(带双孔塞)、锥形瓶、玻璃片、长颈漏斗、集气瓶.
故答案为:
①小曼,碳酸钙与稀盐酸反应生成的CO2气体逸出烧杯,所以剩余的生成物的质量比反应物的总质量减少了.
②HCl+NaOH=NaCl+H2O
③长颈漏斗、集气瓶.
点评:在设计验证质量守恒的实验时要考虑实验在密闭容器中进行,组装装置时注意实验的准确性和安全性.

练习册系列答案
相关题目
据报道一些国家正在试用碳酸水浇灌某些植物,其主要作用是( )
| A、调节土壤的pH,改良酸性土壤 |
| B、促进植物的光合作用 |
| C、促进植物的早熟 |
| D、在大气层中形成温室 |