��Ŀ����
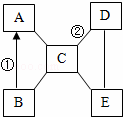
��ͼ�Ǽס��ҡ����������ʵ��ܽ�����ߣ�
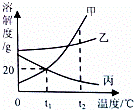
��1�����нӽ����͵ı�������Һ��ʹ���ɱ�����Һ�ķ����У��ټ�������ʣ��ں��������ܼ�����������
��2��t2��ʱ�����ұ����������ܽ����С�����˳����������
��3���μ�����صľ����С������̼����ɹ�Ρ��Ľᾧ�����������̵��ġ�������ܽ��������ͼ�е��������ƣ�
��4����t1��ʱ����15g�����ʷ���50gˮ�У�����ܽ�������Һ��������g��
��5��t1��ʱ�������ұ��������ʵı�����Һ������t2�棬������Һ���ݼ������������ɴ�С��˳����������
| �����ܽ�����������ã��ᾧ��ԭ������������Ӧ�ã�������Һ�Ͳ�������Һ�ת��ķ��������ʵ������������ܽ��Ժ��ܽ�ȵĹ�ϵ�� | |
| ר�⣺ | ��Һ����Һ���ܽ�ȣ� |
| ������ | ��1��������Һ�Ͳ�������Һ֮������ת���� ��2���������ʵ��ܽ�����߿����ж�ijһ�¶�ʱ�����ܽ�ȵĴ�С�� ��3�������̼˵�������ʵ��ܽ�����¶�Ӱ��ϴ�����ɹ�Σ�˵�������ʵ��ܽ�����¶�Ӱ���С�� ��4���������ʵ��ܽ�����߿����ж�ijһ�¶�ʱ�õ������������ܽ���һ���������ܼ����γ���Һ�������� ��5��������Һ��������������=��100%�� |
| ��� | �⣺��1�������ܽ�������¶ȵ����߶���С��Ҫʹ�ӽ����͵ı�������Һ��ɱ�����Һ�ķ����У���������ʣ����������ܼ��������¶ȣ� ��������¶ȣ� ��2��t2��ʱ�����ұ����������ܽ����С�����˳���DZ����ң��ף� ��������ң��ף� ��3����ȡ�����̡����˵�������ʵ��ܽ�����¶�Ӱ��ϴ����ܽ��������ͼ�еļ����ƣ� ����ף� ��4����t1��ʱ�����ܽ����20g����15g�����ʷ���50gˮ�У�ֻ��1 ���60�� ��5��t1��ʱ�����ұ��������ʵı�����Һ������������ϵ�ǣ��ң���=����������t2�棬������Һ�У��Һͼ������������䣬�������������ǣ��ң��ף���Ϊ����t2����ܽ��С��t1��ʱ�ܽ�ȣ���˱�����������С�ڼף����������ɴ�С��˳�����ң��ף����� ����ң��ף����� |
| ������ | �ܽ�������ܶ����ر�ʾ���ܽ�ȱ仯�Ĺ��ɣ����ܽ�����߿��Կ�����ͬһ�����ڲ�ͬ�¶��µ��ܽ�Ȳ�ͬ��ͬһ�¶��£���ͬ���ʵ��ܽ�ȿ�����ͬ��Ҳ���ܲ�ͬ���¶ȶԲ�ͬ���ʵ��ܽ��Ӱ�첻ͬ�� |
��

 ���Ͱ�ͨ������ϵ�д�
���Ͱ�ͨ������ϵ�д� �ٷ�ѧ����ҵ��������ϵ�д�
�ٷ�ѧ����ҵ��������ϵ�д����и��������ǰ����ʡ������������˳�����е��ǣ�������
| �� | A�� | ��������ˮ�������� | B�� | ����������������Һ���� |
| �� | C�� | �����ɱ�����ʯ�� | D�� | ʯī����ʯ�ҡ�ʯ�� |
��һ���ܱյ��������мס��ҡ��������������ʣ���һ�������·�Ӧһ��ʱ�䣬��÷�Ӧǰ������ʵ��������±���
| ���� | �� | �� | �� | �� |
| ��Ӧǰ����/g | 24 | 10 | ���� | 6 |
| ��Ӧ������/g | 8 | 10 | 24 | 2 |
�Ը÷�Ӧ��������������ȷ���ǣ�������
| �� | A�� | �ס����Ƿ�Ӧ��������������� |
| �� | B�� | ����ֵ��8 |
| �� | C�� | ��Ӧ�мס����������ʱ仯����������4��1 |
| �� | D�� | ��һ���Ǹ÷�Ӧ�Ĵ��� |
���ά���ɶ������裨SiO2���Ƴɵģ�������̼�й�Ԫ�صĻ��ϼ�Ϊ��������
| �� | A�� | +1 | B�� | +2 | C�� | +3 | D�� | +4 |
����г�ȥ���������������ʵķ�����������ǣ�������
| ѡ�� | ���� | �������� | ��ȥ���ʵķ��� |
| A | ���� | ���� | �����建��ͨ������������ͭ�� |
| B | ������ | ̼��� | �������� |
| C | �Ȼ�����Һ | ���� | �ӹ�������������Һ |
| D | �Ȼ�����Һ | �Ȼ�þ | �ӹ�������������Һ�����ˡ�������Һ�м�����ϡ��������ҺpH=7 |
| �� | A�� | A | B�� | B | C�� | C | D�� | D |
 0g�ܽ⣬����ܽ�������Һ����60g��
0g�ܽ⣬����ܽ�������Һ����60g��