题目内容
16.在分子、原子核、质子、中子、电子、阳离子、阴离子等微粒中,找出符合下列条件的微粒,填在相应空格上.(1)能直接构成纯净物的是分子
(2)带正电核的是质子、原子核、阳离子
(3)在同一原子中电荷数目相等的是质子和电子
(4)相对原子质量=质子数+中子数.
分析 根据构成物质的微粒,分子、原子的定义,微粒的质量、电性及电量等分析回答.
解答 解:(1)分子能直接构成纯净物.
(2)带正电荷的是质子、原子核、阳离子.
(3)同一原子中数目相等的粒子是质子和电子.
(4)相对原子质量等于质子数+中子数.
故答案为:(1)分子.(2)质子、原子核、阳离子.(3)质子和电子.(4)质子、中子
点评 本题考查学生对化学中微粒的电性,性质、大小等知识的理解,并能在解题中灵活应用的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
7.如图图示实验操作中,正确的是( )
| A. | 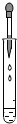 滴加液体 | B. |  往试管加入固体 | C. |  倾倒液体 | D. | 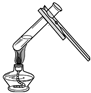 加热液体 |
4.下列各组物质中,必须利用化学性质的不同才能区别的是( )
| A. | 水和食醋 | B. | 铜片和铝片 | C. | 氧气和二氧化碳 | D. | 铁粉和食盐 |
11.酸、碱、盐在工农业生产和日常生活中的应用广泛,促进了人类文明的进步和社会的可持续发展.
(1)下列物质放在敞口容器中一段时间后,会变质且溶液质量明显增加的是C(填字母).
A.食盐水 B.浓硫酸 C.烧碱溶液 D.石灰水
(2)在铁制品表面镀铬(Cr)可以防止铁生锈,工业上获取镀铬原料三氧化铬的化学反应方程式为:Na2Cr2O7+X 2CrO3+Na2SO4+H2O,其中X的化学式为H2SO4.
(3)兴趣小组在进行酸碱中和反应的实验时,向烧杯中的氢氧化钠溶液中滴加稀盐酸后,发现忘记滴加指示剂.甲同学从烧杯中取少量反应后的溶液于一支试管中,并向其中滴加几滴无色酚酞溶液,振荡,观察到酚酞溶液不变色.请写出该氢氧化钠溶液与稀盐酸反应的化学方程式NaOH+HCl═NaCl+H2O.
【猜想与假设】
甲同学:反应后稀盐酸过量,溶液呈酸性;
乙同学:反应后氢氧化钠过量,溶液呈碱性;
丙同学:恰好完全反应,溶液显中性.
甲、丙两位同学经过讨论后觉得乙同学的猜想不正确,两位同学的理由是什么?
【设计实验】请你帮甲同学设计实验来验证他的猜想是成立的.
(4)将100g稀盐酸逐滴滴入100g 8%的氢氧化钠溶液中,测得溶液的pH为7,那么所得溶液中溶质的质量分数是多少?
(1)下列物质放在敞口容器中一段时间后,会变质且溶液质量明显增加的是C(填字母).
A.食盐水 B.浓硫酸 C.烧碱溶液 D.石灰水
(2)在铁制品表面镀铬(Cr)可以防止铁生锈,工业上获取镀铬原料三氧化铬的化学反应方程式为:Na2Cr2O7+X 2CrO3+Na2SO4+H2O,其中X的化学式为H2SO4.
(3)兴趣小组在进行酸碱中和反应的实验时,向烧杯中的氢氧化钠溶液中滴加稀盐酸后,发现忘记滴加指示剂.甲同学从烧杯中取少量反应后的溶液于一支试管中,并向其中滴加几滴无色酚酞溶液,振荡,观察到酚酞溶液不变色.请写出该氢氧化钠溶液与稀盐酸反应的化学方程式NaOH+HCl═NaCl+H2O.
【猜想与假设】
甲同学:反应后稀盐酸过量,溶液呈酸性;
乙同学:反应后氢氧化钠过量,溶液呈碱性;
丙同学:恰好完全反应,溶液显中性.
甲、丙两位同学经过讨论后觉得乙同学的猜想不正确,两位同学的理由是什么?
【设计实验】请你帮甲同学设计实验来验证他的猜想是成立的.
| 实验步骤 | 实验现象 | 实验结论 |
| 取反应后的溶液适量于试管中,滴加碳酸钠溶液 | 产生气泡 | 甲同学猜想成立 |
6.下列过程中没有发生化学变化的是( )
| A. | 木材燃烧 | B. | 湿衣服晾干 | ||
| C. | 葡萄酿酒 | D. | 吃进的食物过一段时间会消化 |