题目内容
8.30℃时硝酸钾的溶解度是45.8克.在此温度下配制的硝酸钾溶液的溶质质量分数为( )| A. | 45.8% | B. | 31.4% | C. | 20% | D. | 无法确定 |
分析 根据溶液中溶质的质量分数=$\frac{溶质的质量}{溶液的质量}×100%$以及饱和溶液中,溶质的质量分数=$\frac{溶解度}{溶解度+100g}×100%$分析解答.
解答 解:因为30℃时硝酸钾的溶解度是45.8g,则该温度下硝酸钾的饱和溶液中溶质的质量分数为:$\frac{45.8g}{45.8g+100g}×100%$=31.4%.所以在该温度下的硝酸钾溶液中的溶质的质量分数最大为31.4%,不饱和溶液中,溶质的质量分数则小于31.4%.而题干中没有说明该溶液是否饱和,所以无法确定该溶液中硝酸钾的质量分数.
故选D.
点评 本题考查了溶质质量分数的计算,难度不大.

练习册系列答案
相关题目
18.钱江晚报报道浙江沿海地区“碘过量”.食物中碘过量易引起患甲状腺疾病,眼球突出,脖子粗大,身体消瘦.因此呼吁大家再也不能吃加碘盐了.某兴趣小组就沿海地区甲状腺疾病患者明显增多的现象,开展了“沿海地区城镇居民甲状腺肿瘤流行病学调查”,提出“浙江沿海地区食盐中是否有必要加碘值得关注”.
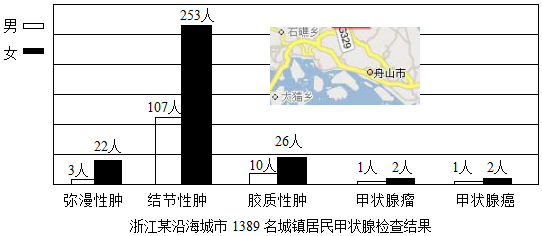
(1)如图是上述调查得到的图表之一,此图表能够反映出的信息是B;
A.该地区居民中患甲状腺瘤的男性人数是女性的一半
B.该地区女性居民更容易患甲状腺疾病
C.该地区居民中甲状腺疾病患者明显增多
D.该地区居民比其他地区居民更容易患甲状腺疾病
(2)碘是合成甲状腺激素的重要原料之一.加碘食盐中的碘以碘酸钾(KIO3)的形式存在,其中碘元素的化合价是+5;
A.+3 B.+5 C.+1 D.-1
(3)如表为某品牌食盐的产品说明,其中“含碘量(35±15)mg/kg”符合国家食盐含碘量的标准.以含碘量35毫克/千克为标准,食盐厂家应该在1千克食盐中加入多少毫克碘酸钾.
(4)“碘是一把双刃剑”,碘过量也会引起甲状腺疾病.初中生每天碘元素适宜摄入量约为0.15毫克,假设碘元素全部来自“加碘盐”,你一天最多可以摄入含碘量为35毫克/千克的食盐多少克. (结果保留一位小数)

(1)如图是上述调查得到的图表之一,此图表能够反映出的信息是B;
A.该地区居民中患甲状腺瘤的男性人数是女性的一半
B.该地区女性居民更容易患甲状腺疾病
C.该地区居民中甲状腺疾病患者明显增多
D.该地区居民比其他地区居民更容易患甲状腺疾病
(2)碘是合成甲状腺激素的重要原料之一.加碘食盐中的碘以碘酸钾(KIO3)的形式存在,其中碘元素的化合价是+5;
A.+3 B.+5 C.+1 D.-1
(3)如表为某品牌食盐的产品说明,其中“含碘量(35±15)mg/kg”符合国家食盐含碘量的标准.以含碘量35毫克/千克为标准,食盐厂家应该在1千克食盐中加入多少毫克碘酸钾.
| 产品标准号 | GB5461-2000 |
| 配 料 | 精制食盐(NaCl) 碘酸钾(KIO3) |
| 质量等级 | 一级 |
| 含 碘 量 | (35±15)mg/kg |
| 食用方法 | 待食品熟后加入碘盐 |
| 储藏方法 | 密封保存、防潮防热 |
| 分装日期 | 见封口 |
19.过量的铁粉放入含有ZnSO4的CuSO4溶液中,充分反应过滤留在滤液中的物质是( )
| A. | Fe SO4 | B. | Fe Cu | C. | Cu SO4 | D. | Fe SO4ZnSO4 |
16.下列物质属于溶液的是( )
| A. | 浑浊的江水 | B. | 植物油和水混合形成的混合物 | ||
| C. | 液态氧 | D. | 酒精与水混合形成的混合物 |
3.从微观的角度认识物质及其变化,更有助于了解物质组成及变化的本质.如图所示图片中不能获取的信息是( )
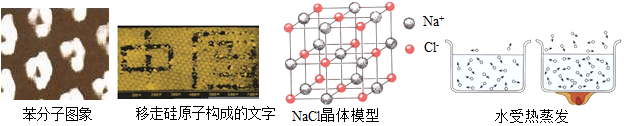

| A. | 构成物质的粒子之间有间隔 | |
| B. | 硅原子是由原子核和电子构成的 | |
| C. | 构成物质的粒子有分子、原子和离子 | |
| D. | 受热水分子运动速率加快 |
13.米皮、凉皮、擀面皮都是河南人夏天喜爱的食品,它们主要由米粉或面粉制成,则米皮、凉皮、擀面皮中富含的营养素中是( )
| A. | 糖类 | B. | 维生素 | C. | 蛋白质 | D. | 油脂 |
17.下列事实与“雾霾”天气增多无关的是( )
| A. | 煤炭的大量燃烧 | B. | 汽车尾气的大量排放 | ||
| C. | 食品包装袋的随意丢弃 | D. | 工厂废气的任意排放 |
18.下列实验操作符合规范且能达到目的是( )
| A. |  测定某溶液的pH | B. |  过滤 | C. |  稀释浓硫酸 | D. |  检验CO32-的存在 |