题目内容
2.2011年唐山市中考实验加试有一个题是四种常见溶液的鉴别,题目要求用酚酞和氯化钙两种人那个也鉴别白醋、食盐水、纯碱溶液和澄清石灰水四种溶液,实验过程汇总的废液都倒入污物瓶,正确实施实验结束后污物瓶内液体呈红色,瓶底有少量白色沉淀.【提出问题】:沉淀一定是碳酸钙,溶液中含有什么物质呢?
【做出猜想】:同学甲根据瓶中溶液呈红色猜想溶液中一定有氢氧化钙,他的想法一说出就遭到同学们的反对,原因是氢氧化钙、氢氧化钠、碳酸钠溶液都显碱性,经过反复讨论大家一致认为:
(1)可以确定该溶液中一定含有水、酚酞和氯化钠.
(2)不能确定的物质由四种:①氢氧化钙②碳酸钠③氯化钙④氢氧化钠.
为进一步确定该溶液中含有的物质,做如下研究:
【进行实验】:同学乙利用试验台上的药品进行实验:取少量废液中的上层清夜于试管中滴入氯化钙溶液,有白色沉淀产生(写实验过程和现象,一种方法即可),发生反应的化学方程式是CaCl2+Na2CO3═CaCO3↓+2NaCl.
【得出结论】:溶液中含有碳酸钠
同时推理得出结论:①溶液中一定不含有氢氧化钙、氯化钙,得到这个结论的理由是碳酸钠会与两者反应生成沉淀;②溶液中还含有氢氧化钠.
【反思与交流】:该废液倒入下水道之前需经中和处理,向其中滴加稀盐酸,至红色褪去(写实验现象)时停止.
分析 【做出猜想】根据氢氧化钙、氢氧化钠、碳酸钠溶液都显碱性进行分析;
(1)根据题中的反应是酚酞和氯化钙鉴别白醋、食盐水、纯碱、澄清石灰水进行分析;
【进行实验】根据实验的出的结论是碳酸钠,然后结合碳酸钠的性质进行分析;
【得出结论】根据钙离子和碳酸根离子会生成碳酸钙沉淀进行分析;
【反思与交流】:根据酸碱中和反应的原理进行分析.
解答 解:【做出猜想】碱性物质都能是酚酞变红色,实施实验结束后污物瓶内液体呈红色,只能说明溶液显碱性,不能说明一定含有氢氧化钙,理由是:氢氧化钙、氢氧化钠、碳酸钠溶液都显碱性;
(1)题中的反应是酚酞和氯化钙鉴别白醋、食盐水、纯碱、澄清石灰水,氯化钠溶液显中性,所以可以确定该溶液中一定含有水、酚酞和氯化钠;
【进行实验】取少量废液中的上层清夜于试管中滴入氯化钙溶液,有白色沉淀产生,碳酸钠和氯化钙反应生成碳酸钙沉淀和氯化钠,化学方程式为:CaCl2+Na2CO3═CaCO3↓+2NaCl,证明含有碳酸钠;
【得出结论】钙离子和碳酸根离子会生成碳酸钙沉淀,所以溶液中含有碳酸钠,同时推理得出结论:①溶液中一定不含有氢氧化钙、氯化钙,得到这个结论的理由是碳酸钠会与两者反应生成沉淀,;②溶液中还含有氢氧化钠;
【反思与交流】该废液倒入下水道之前需经中和处理,向其中滴加稀盐酸,至红色褪去时停止.
故答案为:【做出猜想】氢氧化钙、氢氧化钠、碳酸钠溶液都显碱性;
(1)氯化钠;
【进行实验】滴入氯化钙溶液,有白色沉淀产生,CaCl2+Na2CO3═CaCO3↓+2NaCl,;
【得出结论】氢氧化钙、氯化钙,碳酸钠会与两者反应生成沉淀,氢氧化钠;
【反思与交流】红色褪去.
点评 实验现象是物质之间相互作用的外在表现,因此要学会设计实验、观察实验、分析实验,为揭示物质之间相互作用的实质奠定基础.

 教学练新同步练习系列答案
教学练新同步练习系列答案 课前课后同步练习系列答案
课前课后同步练习系列答案| 实验内容 | 实验设计 | |
| A | 验证某溶液为稀盐酸 | 先测溶液的pH<7,再加入锌粒 |
| B | 提纯久置变质的NaOH溶液 | 加入足量CaCl2溶液,充分反应后,过滤 |
| C | 除去H2中混有的少量水蒸气、HCl | 先通过浓H2SO4,再通过NaOH溶液 |
| D | 分离CO2、CO混合物 | 先用NaOH溶液吸收掉CO2分离出CO,再向该NaOH溶液加足量稀盐酸“释放”出CO2 |
| A. | A | B. | B | C. | C | D. | D |
| A. | CO2 | B. | H2SO4 | C. | Na2CO3 | D. | HCl |
【进行实验】
| 操作步骤 | 实验现象 | 实验结论 |
| 分别用A、B两支试管取少量样品,然后各加入适量澄清石灰水 | A中无明显现象 B中有白色沉淀 | A中的物质是氢氧化钠溶液 B中的物质是碳酸钠溶液 |
【提出问题】反应后滤液中溶质的成分是什么?
【猜想假设】甲同学的猜想:只含有NaOH;乙同学猜想:含有NaOH和Ca(OH)2;丙同学猜想:含有NaOH、Ca(OH)2、Na2CO3;你的猜想:含有NaOH、Na2CO3.
上述猜想中,你认为不合理的猜想是丙(填“甲”“乙”或“丙”),理由是Ca(OH)2与Na2CO3会继续反应,不能共存.
【实验探究】请你设计一个简单的实验来验证“你的猜想”是正确的.
| 实验步骤 | 实验现象 | 实验结论 |
| 取样于试管中加入,再加入稀盐酸 | 有气泡产生 | 猜想成立 |
在分析化学反应后所得物质的成分时,除考虑生成物外还需考虑:反应物的量,通过以上探究,你认为应怎样处理上述实验后的废液才能倒入下水道?
| A. | 将氯化氢和SO2分别通入石蕊试液中,溶液都变为红色,所以它们都是酸类物质 | |
| B. | 饱和溶液有晶体析出,若溶剂质量不变,则溶液的浓度一定变小 | |
| C. | 一氧化碳和氢气都能夺取氧化铜中的氧,它们都具有还原性 | |
| D. | 复分解反应中有沉淀、气体或水生成,所以有上述物质生成的反应就是复分解反应 |
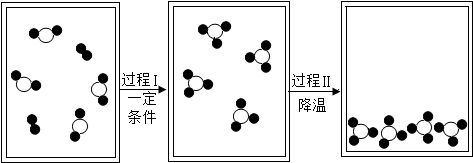
| A. | XY+Y2═2M | B. | 2XY+Y2═2M | C. | 4XY+Y2═2M | D. | XY+2Y2═2M |