题目内容
10.根据下列事实写出有关的化学方程式:(1)将生锈的铁钉放入过量的稀硫酸中,铁锈溶解,溶液呈黄色,不一会儿,又看到铁钉表面出现气泡.(2 个)
(2)生活中,我们常用食醋来清洗水壶内壁结成的水垢(水垢的主要成分是碳酸钙).
分析 根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤进行书写.
解答 解:(1)铁锈的主要成分是氧化铁,能与稀硫酸反应生成硫酸铁和水,反应现象为:铁锈逐渐消失,无色溶液变成黄色,反应的化学方程式为:Fe2O3+3H2SO4=Fe2(SO4)3+3H2O;铁锈完全消失后,铁与稀硫酸反应生成硫酸亚铁和氢气,反应的化学方程式为:Fe+H2SO4=FeSO4+H2↑.
故答案为:Fe2O3+3H2SO4=Fe2(SO4)3+3H2O;Fe+H2SO4=FeSO4+H2↑.
(2)水垢的主要成分是碳酸钙,碳酸钙与醋酸反应生成醋酸钙、水和二氧化碳气体,故答案为:2CH3COOH+CaCO3=(CH3COO)2Ca+H2O+CO2↑.
点评 本题难度不大,考查学生根据反应原理书写化学方程式的能力,掌握化学方程式的书写方法即可正确解答本题.

练习册系列答案
 导学全程练创优训练系列答案
导学全程练创优训练系列答案
相关题目
19.密闭容器内有A、B、C、D四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下.下列说法正确的是( )
| 物 质 | A | B | C | D |
| 反应前质量/g | 19.7 | 8.7 | 31.6 | 0.4 |
| 反应后质量/g | 待测 | 17.4 | 0 | 3.6 |
| A. | 物质C一定是化合物,物质D一定是单质 | |
| B. | 反应后密闭容器中A的质量为19.7 g | |
| C. | 若物质A与物质C的相对分子质量之比为197:158,则反应中A与C的化学计量数之比为l:2 | |
| D. | 反应过程中,物质B与物质D变化的质量比为87:36 |
20.在密闭容器中盛有H2、O2、Cl2混合气体,通过电火花引燃,气体恰好完全反应,冷却至室温后,所得液体产物中HCl的质量分数为12.6%,则容器中原有H2、O2、Cl2分子个数比为(已知H2能在Cl2中燃烧生成HCl)( )
| A. | 6:3:2 | B. | 9:6:1 | C. | 10:6:1 | D. | 29:14:1 |
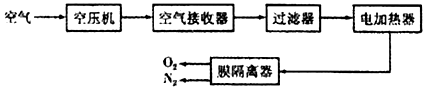
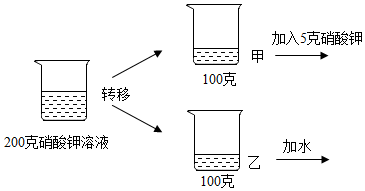
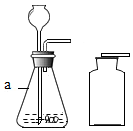 下列是关于二氧化碳和氧气实验室制取的实验,请回答下列问题:
下列是关于二氧化碳和氧气实验室制取的实验,请回答下列问题: