题目内容
13.下列实验不能达到实验目的是( )| A. | 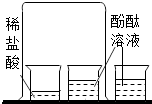 探究分子的运动 | B. | 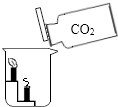 证明CO2密度比空气的大 | ||
| C. | 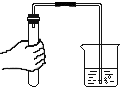 检查装置的气密性 | D. | 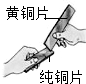 比较合金和纯金属的硬度 |
分析 A、根据稀盐酸显酸性,不能使酚酞溶液变色,进行分析判断.
B、根据装置内的现象为下层的蜡烛先熄灭、上层的蜡烛后熄灭,进行分析判断.
C、根据检查装置气密性的方法进行分析判断.
D、根据合金的性质,进行分析判断.
解答 解:A、稀盐酸显酸性,不能使酚酞溶液变色,实验无明显变化,不能用于探究分子的运动,故选项方案不能达到实验目的.
B、装置内的现象为下层的蜡烛先熄灭、上层的蜡烛后熄灭,说明二氧化碳的密度比空气的大,故选项方案能达到实验目的.
C、检查装置气密性的方法:把导管的一端浸没在水里,双手紧贴容器外壁,若导管口有气泡冒出,装置不漏气,故选项方案能达到实验目的.
D、采用相互刻划的方法,可以比较合金和纯金属的硬度,故选项方案能达到实验目的.
故选:A.
点评 本题难度不是很大,化学实验方案的设计是考查学生能力的主要类型,同时也是实验教与学难点,在具体设计时要对其原理透彻理解,可根据物质的物理性质和化学性质结合实验目的进行分析判断.

练习册系列答案
相关题目
3.下列实验操作正确的是( )
| A. | 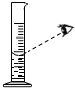 读取体积 | B. | 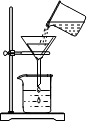 过滤 | C. |  套橡胶管 | D. |  熄灭酒精灯 |
4.下列属于复合肥的是( )
| A. | NH4 NO3 | B. | KHCO3 | C. | KH2PO4 | D. | NH4 Cl |
5.观察下面反应的微观示意图,下列说法错误的是( )


| A. | 化学反应前后各元素的化合价均保持不变 | |
| B. | W物质中碳元素的质量分数为80% | |
| C. | 参加反应的X、Y两物质的粒子个数比为3:4 | |
| D. | 该反应属于置换反应 |
6.“低钠盐”可以控制钠的摄入量从而防治高血压等疾病.制备“低钠盐”是在食盐中用NaCl按照配方比例添加食用KCl.国内某些生产厂家为改变“低钠盐”口味还会加入少量镁盐(仅限MgSO4或MgCl2).
(1)测得某“低钠盐”样品a中只含有NaCl和KCl,该样品中的NaCl和KCl溶于水时解离出的阴离子都是Cl-(填离子符号).
(2)探究某“低钠盐”样品b中是否添加有镁盐,以及添加的是何种镁盐?
【猜想】I、不含镁盐Ⅱ、含有硫酸镁Ⅲ、含有氯化镁
【进行实验】

(3)请完成如表(已知BaSO4是难溶于水和酸的白色固体):
(1)测得某“低钠盐”样品a中只含有NaCl和KCl,该样品中的NaCl和KCl溶于水时解离出的阴离子都是Cl-(填离子符号).
(2)探究某“低钠盐”样品b中是否添加有镁盐,以及添加的是何种镁盐?
【猜想】I、不含镁盐Ⅱ、含有硫酸镁Ⅲ、含有氯化镁
【进行实验】

(3)请完成如表(已知BaSO4是难溶于水和酸的白色固体):
| 假设和现象 | 判断和化学方程式 | |
| ① | 若现象a为白色沉淀 | 则猜想I不成立. |
| ② | 若现象a为产生白色沉淀, 现象b为无明显现象. | 则猜想Ⅲ成立.写出无色溶液B与硝酸中和反 应的化学方程式NaOH+HNO3=NaNO3+H2O. |
| ③ | 若现象a、b均 为:产生白色沉淀 | 则猜想Ⅱ成立.写出无色溶液B与硝酸钡溶液 反应的化学方程式Ba(NO3)2+Na2SO4=BaSO4↓+2NaNO3. |